
 |
Experiment des MonatsChemikalien-Index |
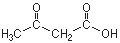 (C4H6O3)
(C4H6O3) 05/2001
05/2001 zurück
zurück
Acetessigsäureethylester, 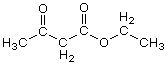 (C6H10O3)
(C6H10O3)
(Acetessigester, Ethylacetoacetat, 3-Oxobutansäure-ethylester) Farblose, leicht ölige Flüssigkeit
mit aromatischem Geruch. Mit Wasser wenig, mit den meisten organischen Lösungsmitteln beliebig mischbar.
Wässrige Lösungen von Acetessigester bilden mit Eisen(III)-Ionen rotviolette Komplexe.
weitere Informationen
 04/2000 - 01/2004
04/2000 - 01/2004
 zurück
zurück
Aceton, 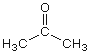 (C3H6O)
(C3H6O)
(Propanon, Dimethylketon) Farbloses, leicht flüchtiges organisches
Lösungsmittel mit aromatischem Geruch, leichtentzündlich.
Läßt sich mit Wasser und fast allen organischen Lösungsmitteln
gut mischen. Aceton ist ein wichtiges Basisprodukt in der chemischen
Industrie (Weltjahresproduktion über eine Million Tonnen) und wird
darüber hinaus als Lösungs- und Extraktionsmittel verwendet.
R 11 -
S 9, 16, 23, 33
weitere Informationen
 08/1999 - 12/1999 -
05/2001 - 09/2007 -
11/2011 - 09/1012 -
09/2018 - 09/2019 -
10/2023 - 02/2026
08/1999 - 12/1999 -
05/2001 - 09/2007 -
11/2011 - 09/1012 -
09/2018 - 09/2019 -
10/2023 - 02/2026
 zurück
zurück
Alizarin S, 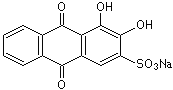 (C14H7NaO7S)
(C14H7NaO7S)
(Alizarin-2-sulfonsäure Natriumsalz) gelbes, in Wasser und Alkohol leicht lösliches Pulver.
Nachweisreagenz für Aluminium, Zirkon u.a.
Säure-Base-Indikator: pH 3,7-5,1 (violett 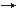 gelb)
weitere Informationen
gelb)
weitere Informationen
 08/2013
08/2013
 zurück
zurück
Alkanna 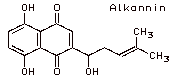
Aus der Alkanna-Pflanze (Alkanna tinctoria) gewonnener Farbstoff, der in organischen
Lösungsmitteln mit roter, in Laugen mit blauer Farbe löslich ist.
Hauptkomponente: Alkannin.
weitere Informationen
 06/1998
06/1998
 zurück
zurück
Aluminium, Al
Unedles Leichtmetall mit sehr großer technischer Bedeutung.
Wird (bei Raumtemperatur) von Sauerstoff, Wasser und verdünnten Säuren
oder Laugen infolge Passivierung kaum angegriffen.
weitere Informationen
 12/2003 - 04/2014
- 01/2023
12/2003 - 04/2014
- 01/2023
 zurück
zurück
Aluminiumkaliumsulfat Dodecahydrat, KAl(SO4)2·12H2O
(Alaun) bildet große farblose oktaedrische Kristalle. Die Wasserlöslichkeit
ist stark temperaturabhängig. Wässrige Lösungen reagieren sauer.
weitere Informationen
 05/2004 - 08/2013
- 01/2019
05/2004 - 08/2013
- 01/2019
 zurück
zurück
Ameisensäure, HCOOH
(Methansäure) Einfachste Carbonsäure, farblose Flüssigkeit
mit stechendem Geruch. Kommt in Giftsekreten einiger Insekten (Waldameise)
und Pflanzen (Brennessel) vor. Sie wurde erstmals 1670 von J. Wray beim
Erhitzen von Ameisen erhalten. Ätzend.
R 35 -
S 2, 23, 26
weitere Informationen
 05/2025
05/2025
 zurück
zurück
Ammoniak-Lösung, NH3 aq
(Ammoniumhydroxid, Salmiakgeist) Lösung von Ammoniak-Gas (NH3)
in Wasser. Reizend.
R 34, 37 -
S 7, 26, 45
weitere Informationen
 12/1999 - 09/2004
- 01/2005 - 08/2012
- 11/2012 - 08/2023
- 08/2024
12/1999 - 09/2004
- 01/2005 - 08/2012
- 11/2012 - 08/2023
- 08/2024
 zurück
zurück
Ammonium-cer(IV)-nitrat, (NH4)2Ce(NO3)6
(Cerammoniumnitrat) bildet orange-rote, gut wasserlösliche Kristalle.
Nachweis-Reagens für Alkohole und Phenole. Brandfördernd, reizend.
R 8, 36/38 - S 22, 28
 09/2007
09/2007
 zurück
zurück
Ammoniumcarbonat, (NH4)2CO3
bildet weiße glänzende Kristalle. In Wasser begrenzt löslich (bei 20oC ca. 20 g / 100 ml),
in organischen Lösungsmitteln praktisch unlöslich.
Hauptbestandteil von Hirschhornsalz, das als Backtriebmittel für dünne Backwaren
(Kekse, Lebkuchen etc.) verwendet wird (beim Backen muß NH3 vollständig entweichen können.
weitere Informationen
 07/2013 - 03/2015
07/2013 - 03/2015
 zurück
zurück
Ammoniumchlorid, NH4Cl
(Salmiak) Wichtigstes Ammoniumsalz, bildet farblose Kristalle. In Wasser gut
(bei 20oC ca. 37 g / 100 ml), in organischen Lösungsmitteln kaum löslich.
Das Salz sublimiert bei 338oC, wobei der Dampf in NH3 und HCl dissoziiert.
Wässrige Lösungen reagieren sauer.
Ammoniumchlorid entsteht als Nebenprodukt beim Solvay-Verfahren zur Soda-Darstellung oder bei
der direkten Umsetzung der Gase NH3 und HCl, z.B. als weißer Belag auf
Flaschen und Türen von Chemikalienschränken, in denen Salzsäure und
Ammoniak-Lösung aufbewahrt werden.
NH4Cl wird vor allem als Elektrolyt in Trockenbatterien verwendet, ist aber auch
an vielen chemisch-technischen Prozessen beteiligt. Gepreßte NH4Cl-Blocks
kommen als Lötstein zum Einsatz. Durch Erhitzen mit dem Lötkolben verdampft
das Salz uns setzt HCl frei, das Oxidschichten auf dem Lötzinn und den
Metalloberflächen zersetzt.
Gesundheitsschädlich, reizend.
R 22, 36 -
S 22, 28
weitere Informationen
 01/2000 - 01/2003
- 02/2010 - 07/2010
01/2000 - 01/2003
- 02/2010 - 07/2010
 zurück
zurück
Ammoniumdichromat, (NH4)2Cr2O7
Orangerote Kristalle, explosionsgefährlich, brandfördernd, reizend,
giftig, vermutlich cancerogen.
R 1, 8, 21, 25, 26, 36/37/38, 41, 43, 46, 49, 50 -
S 28, 35, 45, 53, 60, 61
weitere Informationen
 01/1998
01/1998
 zurück
zurück
Ammonium-eisen(II)-sulfat Hexahydrat, (NH4)2Fe(SO4)2 · 6 H2O
(Mohrsches Salz) bildet hellgrüne, gut wasserlösliche Kristalle.
Im Mohrschen Salz ist Eisen(II) erheblich stabiler als in anderen Salzen. Auch in der
Lösung des Doppelsalzes erfolgt die Oxidation langsamer als sonst. Reizend.
R 36/37/38 -
S 24/25/26
weitere Informationen
 12/2007
12/2007
 zurück
zurück
Ammonium-eisen(III)-sulfat Dodecahydrat, NH4Fe(SO4)2 · 12 H2O
(Eisenalaun) bildet große, hellviolette Kristalle. Löst sich sehr gut in Wasser
mit schwach gelber Farbe.
S 24/25
weitere Informationen
 01/2002
01/2002
 zurück
zurück
Ammoniummolybdat Tetrahydrat, (NH4)6Mo7O24 · 4 H2O
farblose, gut wasserlösliche Kristalle. Wichtiges Nachweisreagens für Phosphate.
Reizend, gesundheitsschädlich.
R 22, 36/37/38 -
S 26, 36
weitere Informationen
 08/2006 - 01/2016
- 06/2021
08/2006 - 01/2016
- 06/2021
 zurück
zurück
Ammoniumnitrat, NH4NO3
Bildet farblose, hygroskopische Kristalle, die in Wasser sehr gut löslich sind.
Das Salz wird hauptsächlich zur Stickstoff-Düngung eingesetzt.
Beim Erwärmen zerfällt Ammoniumnitrat in N2O und Wasser.
Bei Initialzündung kann diese Zersetzung explosionsartig erfolgen, es kam
bereits mehrfach zu katastrophalen Unfällen.
Explosionsgefährlich, brandfördernd.
R 8 -
S 15, 17
weitere Informationen
 01/2000 - 07/2003
01/2000 - 07/2003
 zurück
zurück
Ammoniumoxalat, (NH4)2(C2O4)
farblose, gut wasserlösliche Kristalle.
Ammonium-Salz der Oxalsäure.
Wichtiges Nachweisreagens für Calcium-Ionen
(Ca2+-Ionen ergeben mit Oxalaten einen weißen Niederschlag)
Gesundheitsschädlich.
R 21/22 -
S 24/25
weitere Informationen
 09/2006 - 12/2007
09/2006 - 12/2007
 zurück
zurück
Ammoniumsulfat, (NH4)2SO4
bildet farblose, nicht hygroskopische, gut wasserlösliche Kristalle.
Die wässrige Lösung reagiert schwach sauer.
weitere Informationen
 01/2005
01/2005
 zurück
zurück
Ammoniumsulfid, (NH4)2S
farblose - in Lösung meist durch Zersetzungsprodukte gelbliche - Verbindung, die deutlich nach Schwefelwasserstoff riecht.
Ammoniumsulfid-Lösungen werden insbesondere im anorganischen Trennungsgang verwendet. Giftig, ätzend und umweltgefährdend.
R 11, 31, 34, 50 -
S 16, 26, 36/37/39, 61
weitere Informationen
 04/2013
04/2013
 zurück
zurück
Ammoniumthiocyanat, NH4SCN
(Ammoniumrhodanid) bildet farblose, hygroskopische, in Wasser und Alkoholen
gut lösliche, blättchenförmige Kristalle. Oberhalb 70°C beginnt
die Umwandlung in Thioharnstoff. Ammoniumthiocyanat wird als Korrosionsinhibitor,
Stabilisator in fotografischen Entwicklern und als Vulkanisationsbeschleuniger
verwendet. Charakteristisch für alle Thiocyanate ist die Bildung tiefroter
Eisen(III)Komplexe. Gesundheitsschädlich.
R 20/21/22, 32 -
S 2, 13
weitere Informationen
 02/2001 - 07/2003
- 01/2011 - 12/2017
02/2001 - 07/2003
- 01/2011 - 12/2017
 zurück
zurück
Amylalkohol
Gemisch aus verschiedenen Pentanolen. Hauptkomponente ist 1-Pentanol.
Farblose Flüssigkeit mit eigenwilligem Geruch.
Mit Wasser kaum, mit anderen Alkoholen, Estern und Ethern sehr gut mischbar.
Amylalkohole entstehen als Nebenprodukt jeder alkoholischen Gärung. Die Fuselöle machen
etwa 0,5% der entstehenden Alkohole aus und bestehen zu 60-80% aus Amylalkoholen, die früher
hieraus gewonnen wurden. Heute erfolgt die Synthese meist durch Hydroformylierung von
Butenen oder Hydrolyse von Chlorpentanen. Leichtentzündlich, reizend.
R 11, 20 -
S 24/25
 02/2001 - 09/2001
02/2001 - 09/2001
 zurück
zurück
Antimon(III)chlorid, (SbCl3)
bildet eine farblose, verformbare, stark hygroskopische Masse mit stechendem Geruch. Löslich in halogenierten
Lösungsmitteln; in Wasser erfolgt sofort Hydrolyse zu SbOCl und SbO(OH).
Ätzend, umweltgefährdend, möglicherweise kanzerogen.
R 34, 51/53 -
S 26, 45, 61
weitere Informationen
 01/2012
01/2012
 zurück
zurück
L-Ascorbinsäure, 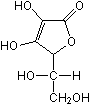 (C6H8O6)
(C6H8O6)
Vitamin C, bildet farblose, gut wasserlösliche Kristalle, schmeckt säuerlich.
Für den Menschen und alle anderen Primaten, sowie für Meerschweinchen essentiell.
Ascorbinsäure kommt in vielen Früchten und Gemüse vor, wird aber
heute überwiegend synthetisch gewonnen. Sie ist ein starkes Reduktionsmittel.
weitere Informationen
 02/2004 - 08/2007 -
10/2011
02/2004 - 08/2007 -
10/2011
 zurück
zurück
Bariumchlorid Dihydrat, BaCl2 · 2 H2O
Farbloses Salz, bildet flache, an der Luft stabile rhomboedrische Kristalle. Giftig.
R 20/22 -
S 28
weitere Informationen
 01/2002 - 12/2014
01/2002 - 12/2014
 zurück
zurück
Bariumhydroxid Octahydrat, Ba(OH)2 · 8 H2O
Farbloses, gut wasserlösliches Salz, wobei die Löslichkeit stark
temperaturabhängig ist. Die wässrige Lösung ist
eine starke Lauge. Giftig und ätzend.
R 20/22, 38 -
S 28
weitere Informationen
 07/2003
07/2003
 zurück
zurück
Bariumnitrat, Ba(NO3)2
Farbloses, wasserlösliches Salz. Gemische mit brennbaren Substanzen sind oft explosionsgefährlich. Giftig und brandfördernd.
R 09, 20/22 -
S 15, 17, 28
weitere Informationen
 01/2023
01/2023
 zurück
zurück
Benzin
Gemisch verschiedener Kohlenwasserstoffe, i. allg. durch Destillation von Rohöl gewonnen,
je nach Typ Siedepunkte zwischen 40o...240oC, leichtentzündlich.
Die wichtigsten als Lösungsmittel verwendeten Fraktionen sind:
Petrolether (Wundbenzin), Pentanfraktion (Siedebereich: 40-65°C)
Ligroin (Leichtbenzin), Heptanfraktion (Siedebereich: 65-100°C)
Waschbenzin, Octanfraktion (Siedebereich: 100-140°C)
Testbenzin, Nonanfraktion (Siedebereich: 135-185°C)
R 11 - S 9, 16, 29, 33
weitere Informationen
 06/1998 - 01/2001 -
02/2002 - 06/2011 -
02/2016 - 10/2023
06/1998 - 01/2001 -
02/2002 - 06/2011 -
02/2016 - 10/2023
 zurück
zurück
Benzylalkohol, 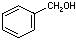 (C7H8O)
(C7H8O)
(Phenylmethanol), farblose, aromatisch riechende Flüssigkeit. In Wasser wenig löslich,
mit den meisten organischen Lösungsmitteln gut mischbar. Leicht zu Benzaldehyd und
weiter zu Benzoesäure oxidierbar. Gesundheitsschädlich.
R 20/22 - S 26
weitere Informationen
 09/2007
09/2007
 zurück
zurück
Benzylchlorid, 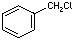 (C7H7Cl)
(C7H7Cl)
(α-Chlor-toluol, Chlormethylbenzol), Reagenz für die organische Synhese, giftig und cancerogen.
R 45, 22, 23, 37/38, 41, 48/22 - S 45, 53
weitere Informationen
 05/2007
05/2007
 zurück
zurück
Bismut(III)nitrat, Bi(NO3)3·5H2O
Wismutnitrat bildet farblose, gut wasserlösliche Kristalle.
Wegen des süßen Geschmacks, wurde das Salz früher als "Bleizucker" bezeichnet.
Wässrige Lösungen reagieren schwach sauer. Giftig.
R 8, 36/38 -
S 15, 17, 26, 28
weitere Informationen
 02/2018
02/2018
 zurück
zurück
Bleiacetat Trihydrat, Pb(CH3COO)2·3H2O
("Bleizucker") bildet große, farblose, gut wasserlösliche Kristalle.
Wegen des süßen Geschmacks, wurde das Salz früher als "Bleizucker" bezeichnet.
Wässrige Lösungen reagieren schwach sauer. Giftig.
R 20/22, 33 -
S 13, 20/21
weitere Informationen
 10/2007
10/2007
 zurück
zurück
Borsäure, H3BO3
Farbloses Pulver oder durchscheinende glänzende Blättchen;
in Wasser und Alkoholen löslich, die wässrige Lösung reagiert schwach sauer.
Beim Erwärmen bildet sich unter Wasserabspaltung Metaborsäure (HBO2)
und schliesslich wasserfreies Boroxid (B2O3).
R 21/22, 36/37/38 -
S 26, 36/37
weitere Informationen
 12/2005 - 12/2022
12/2005 - 12/2022
 zurück
zurück
Brenzkatechin 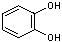 (C6H6O2)
(C6H6O2)
(1,2-Dihydroxybenzol) bildet farblose, gut wasserlösliche Kristalle. Gut löslich
in den meisten organischen Lösungsmitteln. Brenzkatechin besitzt stark bakterizide
Wirkung und ist ein starkes Reduktionsmittel. Es verfärbt sich leicht und sollte
luft- und lichtgeschützt aufbewahrt werden.
Gesundheitsschädlich, reizend. R 22, 38 - S 24
weitere Informationen
 01/2004
01/2004
 zurück
zurück
Brom, Br2
Dunkel-rotbraune Flüssigkeit mit hoher Dichte (r = 3,21 g/ml).
Brom und Quecksilber sind die einzigen bei Raumtemperatur flüssigen Elemente.
Bromdämpfe sind noch in einer Verdünnung von 1 : 100 000 gut wahrnehmbar, daher
wurde der Name des Elementes von bromos (grch. = Gestank) abgeleitet.
Flüssiges Brom und Bromdämpfe sind stark ätzend und sehr giftig.
Brom verursacht auf der Haut schwere, schlecht heilende Verätzungen. Eingeatmete
Bromdämpfe können noch bei Konzentrationen um 10 ppm schwere Lungenschäden
hervorrufen. Bromdämpfe können mit Ammoniak abgefangen werden.
R 26, 35 - S 7/9, 26
weitere Informationen
 02/2005
02/2005
 zurück
zurück
Bromthymolblau 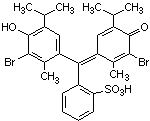 (C27H28Br2O5S)
(C27H28Br2O5S)
(3,3'-Dibromthymolsulfonphthalein) Rosafarbenes, in Alkohol gut, in Wasser wenig lösliches Pulver.
Säure-Base-Indikator: pH 6,0-7,6 (gelb  blau)
blau)
weitere Informationen
 11/2000 - 03/2003
11/2000 - 03/2003
 zurück
zurück
Bromwasser, Br2
Gesättigte Lösung von Brom in Wasser (ca. 3,5%).
Ätzend. R 26, 35 - S 7/9, 26
weitere Informationen
 04/2000 - 10/2018
04/2000 - 10/2018
 zurück
zurück
n-Butanol, 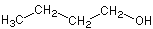 (C4H10O)
(C4H10O)
(1-Butanol) organische Lösungsmittel mit eigenwilligem, an Fuselöle
erinnernden Geruch. In Wasser nur begrenzt löslich, mit den meisten organischen
Lösungsmitteln beliebig mischbar. n-Butanol wird leicht über Butanal zu
Buttersäure oxidiert, älteres Butanol riecht daher oft nach ranziger Butter.
Leichtentzündlich, gesundheitsschädlich beim Einatmen.
R 10, 20 -
S 9, 16
weitere Informationen
 06/2008
06/2008
 zurück
zurück
tert.-Butanol, 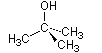 (C4H10O)
(C4H10O)
(2-Methyl-2-propanol, Trimethylcarbinol) Bei Raumtemperatur feste
(Smp = 26oC) organische Substanz mit campherähnlichem Geruch.
Mit Wasser beliebig mischbar, löslich in Ethanol und Diethylether.
tert.-Butanol dient als Esterkomponente, Antiklopfmittel und wird zur
Vergällung von Ethanol eingesetzt.
Leichtentzündlich, gesundheitsschädlich beim Einatmen.
R 11, 20 -
S 9, 16
weitere Informationen
 07/1999
07/1999
 zurück
zurück
Butanon, 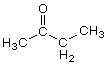 (C4H8O)
(C4H8O)
(Ethyl-Methyl-Keton, Methylethylketon = MEK) Farbloses, leicht flüchtiges organisches
Lösungsmittel mit fruchtigem Geruch, leichtentzündlich;
mit Wasser und fast allen organischen Lösungsmitteln vollständig mischbar.
Vergällungsmittel für Ethanol.
R 11, 36, 66, 67 -
S 9, 16
weitere Informationen
 09/1012
09/1012
 zurück
zurück
tert.-Butylchlorid, 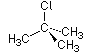 (C4H9Cl)
(C4H9Cl)
(2-Chlor-2-methyl-propan), organisches Lösungsmittel, leichtentzündlich.
R 11 - S 9, 16, 29
weitere Informationen
 05/2007
05/2007
 zurück
zurück
Calciumchlorid, CaCl2
kommt mit unterschiedlichen Kristallwassergehalten vor. Im Handel sind das wasserfreie, sowie das Dihydrat und
das Hexahydrat. Alle Varianten sind hygroskopisch und bilden farblose bzw. weiße Kristalle, die gut
wasserlöslich sind. Wasserfreies CaCl2 wird als Trockenmittel verwendet. Reizend.
R 36 -
S 22, 24
weitere Informationen
 01/2010 - 12/2014
- 06/2021
01/2010 - 12/2014
- 06/2021
 zurück
zurück
Calciumhydroxid, Ca(OH)2
(gelöschter Kalk) weißes Pulver oder farblose Kristalle,
in Wasser nur wenig löslich mit stark alkalischer Reaktion.
Ca(OH)2 entsteht aus CaO (gebrannter Kalk) beim "Kalklöschen".
Die Hauptmenge wird zu Mörtel verarbeitet. Dazu wird Ca(OH)2
(früher wurde CaO verwendet) mit Wasser und Sand versetzt. Beim Aushärten
nimmt der Mörtel CO2 aus der Luft auf, es entsteht CaCO3.
Im Labor kann eine filtrierte wässrige Lösung von Ca(OH)2
("Kalkwasser") zum CO2-Nachweis verwendet werden. Ätzend.
R 38 -
S 22, 28
weitere Informationen
 06/2004 - 10/2007
- 09/2023
06/2004 - 10/2007
- 09/2023
 zurück
zurück
Campher, 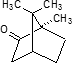 (C10H16O)
(C10H16O)
(Kampfer), kommt in zwei Isomeren (und auch als Racemat) in verschiedenen Pflanzen vor.
Namensgebend ist der Kampferbaum (Cinnamomum camphora), dessen Rinde und Harz (+)-Campher enthält.
Campher ist in den meisten organischen Lösungsmitteln gut löslich, wirkt reizend und ist
leichtentzündlich. Er besitzt einen hohen Dampfdruck, die Dämpfe können explosionsfähige
Gemische mit Luft bilden.
R 11, 36/37/38
weitere Informationen
 09/2015
09/2015
 zurück
zurück
Chlorbenzol, 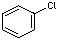 (C6H5Cl)
(C6H5Cl)
(Phenylchlorid), organisches Lösungsmittel, gesundheitsschädlich, umweltgefährdend.
R 10, 20, 51/53 - S 24/25, 61
weitere Informationen
 05/2007
05/2007
 zurück
zurück
1-Chlorbutan,  (C4H9Cl)
(C4H9Cl)
(n-Butylchlorid), organisches Lösungsmittel, leichtentzündlich.
R 11 - S 9, 16, 29
 05/2007
05/2007
 zurück
zurück
Chloressigsäure, CH2Cl-COOH
(Chlorethansäure, Monochloressigsäure) Farblose Kristalle mit stechendem Geruch (Smp. 61°C), gut wasserlöslich.
Ätzend und giftig.
R 10, 25, 34, 50 - S 2, 23, 26, 45, 61
weitere Informationen
 05/2025
05/2025
 zurück
zurück
Chloroform, CHCl3
(Trichlormethan), organisches Lösungsmittel. Es besitzt ein sehr
großes Lösungsvermögen für Fette und viele andere
unpolare organische Stoffe. Chloroform wirkt stark narkotisch, ist aber giftig
(verursacht vor allem schwere Leberschäden) und möglicherweise carcinogen.
R 20, 40 - S 2, 24/25
weitere Informationen
 06/1998 - 07/2004
- 05/2006 - 01/2012
06/1998 - 07/2004
- 05/2006 - 01/2012
 zurück
zurück
Citronensäure  Zitronensäure
Zitronensäure
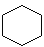 (C6H12)
(C6H12) 10/2018
10/2018 zurück
zurück
Cyclohexen, 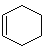 (C6H10)
(C6H10)
organische Verbindnung mit unangenehm benzinartigem Geruch; leichtentzüdlich.
Wird durch Dehydratisierung aus Cyclohexanol gewonnen.
R 11 - S 9, 16, 33
weitere Informationen
 10/2018
10/2018
 zurück
zurück
L-Cystein 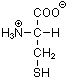 (C3H7NO2S)
(C3H7NO2S)
(R-2-Amino-3-mercapto-propansäure), proteinogene Aminosäure.
Farbloser, in Wasser, Alkohol und Essigsäure gut löslicher Feststoff.
In unpolaren Lösungsmitteln unlöslich.
L-Cystein kann leicht oxidiert werden. Es erfolgt Dimerisierung unter
Bildung einer S-S-Bindung = Cystin.
weitere Informationen
 02/2005 - 05/2005 -
10/2011 - 09/1012
02/2005 - 05/2005 -
10/2011 - 09/1012
 zurück
zurück
Dichloressigsäure, CHCl2-COOH
(Dichlorethansäure) Farblose Flüssigkeit mit stechendem Geruch, gut wasserlöslich.
Ätzend und giftig.
R 10, 25, 34, 50 - S 2, 23, 26, 45, 61
weitere Informationen
 05/2025
05/2025
 zurück
zurück
Diethylether, 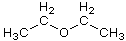 (C4H10O)
(C4H10O)
Organisches Lösungsmittel mit sehr hohem Dampfdruck. Siedepunkt: 34,5°C.
Hochentzündlich, bildet mit Luft bereits bei Konzentrationen ab 1,8%
explosible Gemische, Selbstentzündung bei 180°C. Kann leicht Peroxide bilden,
daher stets in dunklen Flaschen über Natriumhydroxid oder Natrium aufbewahren.
Die Dämpfe wirken narkotisch, Diethylether kann daher in der Medizin als
Inhalationsnarkotikum verwendet werden.
R 12, 19 - S 9, 16, 29, 33
weitere Informationen
 09/2001
09/2001
 zurück
zurück
Dimethylglyoxim Dinatriumsalz Octahydrat 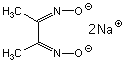 (C4H8N2O2 · 8 H2O)
(C4H8N2O2 · 8 H2O)
(Diacetyldioxim), farbloses Pulver, Nachweisreagenz insbesondere
für Nickel.
S 22, 24/25
weitere Informationen
 06/1999 - 01/2024
06/1999 - 01/2024
 zurück
zurück
2,2'-Dinitro-5,5'-dithio-dibenzoesäure 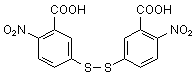 (C14H8N2O8S2)
(C14H8N2O8S2)
(5,5'-Dithiobis(2-nitrobenzoesäure), DTNB), gelblicher Feststoff, in Wasser kaum löslich.
Nachweisreagenz für Cystein: Ellmann-Reagenz
 02/2005
02/2005
 zurück
zurück
2,4-Dinitrophenylhydrazin 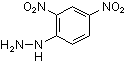 (C6H6N4O4)
(C6H6N4O4)
(DNPH-Reagenz), dunkelroter Feststoff, in Wasser nahezu unlöslich.
Nachweisreagenz für Carbonylverbindungen. In trockener Form explosiv, kommt nur angefeuchtet in den Handel (Wassergehalt ca. 30%)
R 2, 22, 36/38 -
S 35
weitere Informationen
 10/2024
10/2024
 zurück
zurück
Eisen, Fe
Wichtiges Gebrauchsmetall.
weitere Informationen
 02/1998 - 07/1998 -
01/2001 - 12/2007 -
01/2013 - 01/2023 -
08/2025
02/1998 - 07/1998 -
01/2001 - 12/2007 -
01/2013 - 01/2023 -
08/2025
 zurück
zurück
Eisen(III)chlorid Hexahydrat, FeCl3 ·
6 H2O
Orangegelbes hygroskopisches Salz, das an der Luft unter Wasseraufnahme zu einer
rotbraunen Lösung zerfließt. Infolge teilweiser Hydrolyse reagiert die
Lösung stark sauer. Ätzend.
R 34 -
S 7/8, 26, 36/37/39, 45
weitere Informationen
 03/1999 - 04/2000 -
06/2000 - 08/2000 -
12/2000 - 02/2001 -
07/2001 - 01/2004 -
05/2005 - 01/2011 -
01/2011 - 10/2011 -
03/2013 - 08/2013 -
04/2015 - 04/2016 -
08/2016
03/1999 - 04/2000 -
06/2000 - 08/2000 -
12/2000 - 02/2001 -
07/2001 - 01/2004 -
05/2005 - 01/2011 -
01/2011 - 10/2011 -
03/2013 - 08/2013 -
04/2015 - 04/2016 -
08/2016
 zurück
zurück
Eisen(III)nitrat Nonahydrat, Fe(NO3)3 · 9 H2O
bildet gelbliche, hygroskopische gut wasserlösliche Kristalle.
Brandfördernd, reizend.
R 8, 36/38 -
S 17, 26
weitere Informationen
 06/2005
06/2005
 zurück
zurück
Eisen(II)sulfat Heptahydrat, FeSO4 · 7 H2O
(Eisenvitriol) Bildet in reinem Zustand hellblaue Kristalle. Meist ist es mit geringen
Mengen Fe(III) verunreinigt und dann hellgrün. Gut wasserlöslich, unlöslich in
Ethanol und Aceton. Eisen(II)sulfat-Kristalle verwittern an der Luft sehr schnell unter
Wasserabgabe und Oxidation zu Eisen(III)sulfat. Gesundheitsschädlich.
R 22 - S 24
weitere Informationen
 10/1999 -
05/2000 - 12/2007
10/1999 -
05/2000 - 12/2007
 zurück
zurück
Essigsäure, 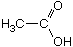 (C2H4O2)
(C2H4O2)
(Ethansäure) Farblose, charakteristisch stechend riechende Flüssigkeit.
Mit Wasser unbegrenzt mischbar. Schmelzpunkt: 16,5°C, Siedepunkt: 118°C.
Reine Essigsäure wird - wegen ihres vergleichsweise hohen Schmelzpunktes -
als Eisessig bezeichnet.
Carbonsäure mit pKS = 4,75. Ätzend.
R 10, 35 - S 2, 23, 26
weitere Informationen
 06/2008 - 02/2009 -
06/2009 - 07/2012 -
12/2013 - 08/2017 -
05/2025
06/2008 - 02/2009 -
06/2009 - 07/2012 -
12/2013 - 08/2017 -
05/2025
 zurück
zurück
Essigsäureanhydrid, 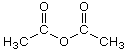 (C4H6O3)
(C4H6O3)
(Acetanhydrid) Farblose, stechend riechende und tränenreizende Flüssigkeit.
Reagiert mit Wasser langsam zu Essigsäure, mit Alkoholen zu Estern. Löslich in
Chlorofom und Diethylether. Ätzend.
R 10, 34 - S 26
weitere Informationen
 05/2006
05/2006
 zurück
zurück
Essigsäureethylester, 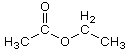 (C4H8O2)
(C4H8O2)
(Ethylacetat, Essigester) Farbloses, flüchtiges, organisches Lösungsmittel mit angenehmem Geruch.
Siedepunkt: 77°C. Dämpfe reizen die Schleimhäute und wirken in
höherer Konzentration narkotisch. Wichtiges Lösungsmittel in der
chemischen Industrie. Leichtentzündlich.
R 11 - S 16, 23, 29, 33
weitere Informationen
 09/2001 - 11/2011 -
08/2017
09/2001 - 11/2011 -
08/2017
 zurück
zurück
Ethanol, C2H5OH
(Äthylalkohol, Weingeist), organisches Lösungsmittel ...,
leichtentzündlich.
Scheint zuweilen auch Probleme zu lösen, doch ist dies meist nur eine
Illusion!
R 11 - S 7, 16
weitere Informationen
 06/1998 - 12/1998 -
01/2001 - 02/2002 -
04/2002 - 02/2003 -
05/2004 - 07/2004 -
07/2006 - 05/2007 -
09/2007 - 08/2009 -
09/2009 - 12/2012 -
10/2014 - 12/2015 -
03/2017 - 02/2023 -
10/2023 - 12/2023 -
02/2026
06/1998 - 12/1998 -
01/2001 - 02/2002 -
04/2002 - 02/2003 -
05/2004 - 07/2004 -
07/2006 - 05/2007 -
09/2007 - 08/2009 -
09/2009 - 12/2012 -
10/2014 - 12/2015 -
03/2017 - 02/2023 -
10/2023 - 12/2023 -
02/2026
 zurück
zurück
Ethylenglykol 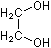 (C2H6O2)
(C2H6O2)
(1,2-Ethandiol, Glykol), Zweiwertiger Alkohol; farblose, viskose, süßlich
schmeckende Flüssigkeit. Ethylenglykol wird heute hauptsächlich durch Hydrolyse von
Ethylenoxid hergestellt und vor allem als Gefrierschutzmittel in Automobilen verwendet: Bei
einem 1:1-Gemisch aus Ethylenglykol und Wasser beginnt die Eisbildung erst bei -40°C.
R 22 - S 2
weitere Informationen
 zurück
zurück
Ferroin 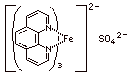 [Fe(C12H8N2)3]SO4
[Fe(C12H8N2)3]SO4
(tris-Phenanthrolin-Eisensulfat), Redox-Indikator, reduziert: rot, oxidiert: blau
(= Ferriin).
weitere Informationen
 05/1998
05/1998
 zurück
zurück
Fluorescein 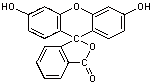 (C20H12O5)
(C20H12O5)
rotbraunes feinkristallines Pulver, in heißem Ethanol löslich, in Wasser und
den meisten organischen Lösungsmitteln praktisch unlöslich. Gut löslich in
Laugen, wobei sich dann eine intensive gelb-grüne Fluoreszenz zeigt. Oft wird daher
das Natriumsalz des Fluoresceins verwendet, überwiegend als Fluoreszenzfarbstoff.
weitere Informationen
 12/2004 - 01/2006 -
07/2025
12/2004 - 01/2006 -
07/2025
 zurück
zurück
Fructose 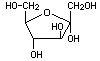 (C6H12O6)
(C6H12O6)
Fruchtzucker, bildet farblose Kristalle. Gut wasserlöslich.
Fructose schmeckt süßer als Glucose.
weitere Informationen
 03/2005 - 02/2006
03/2005 - 02/2006
 zurück
zurück
Fuchsin 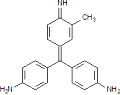 (C20H19N3)
(C20H19N3)
roter Triphenylmethanfarbstoff, in Ethanol löslich. Ergibt mit schwefliger Säure
Schiffs Reagenz zum Nachweis von Aldehyden.
weitere Informationen
 08/2009
08/2009
 zurück
zurück
Gallussäure 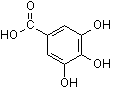 (C7H6O5)
(C7H6O5)
(3,4,5-Trihydroxybenzoesäure). Farblose Kristalle, die in kaltem Wasser
nur gering, in heißem Wasser gut löslich sind (bei 20°C: 1,2g/100ml,
bei 100°C: 30g/100ml). In Ethanol und Aceton gut, in unpolaren Lösungsmitteln
nicht löslich. Mit Eisen(III)-Salzen entsteht ein blauschwarzer
Niederschlag. Gallussäure ist ein wichtiger Bestandteil der
Tannine. Sie wird außer als Gerbstoff und für
Tinten auch als wichtige Synthese-Grundsubstanz benötigt.
S 22, 24/25
weitere Informationen
 01/2002 - 04/2015
01/2002 - 04/2015
 zurück
zurück
Gelatine
Gelatine besteht aus einem Gemisch langkettiger, teilweise hydrolysierter,
Proteine. Sie wird aus Kollagen (meist von Knochen) durch Behandeln mit
verdünnten Mineralsäuren und Auskochen mit Wasser gewonnen.
Gelatine zeichnet sich durch ein hohes Quellvermögen aus, wobei sie die
5 - 10fache Menge Wasser aufnehmen kann. Verwendet wird Gelatine als
Verdickungsmittel in Lebensmitteln (Gelees, Sülzen, Pudding ...),
Bindemittel (Pharmazeutika, Kosmetika, Fotografie ...) sowie in der
Mikrobiologie als Nährmedium.
weitere Informationen
 07/1998 - 07/2002
- 05/2010
07/1998 - 07/2002
- 05/2010
 zurück
zurück
Glucose 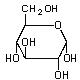 (C6H12O6)
(C6H12O6)
Traubenzucker. Häufigste organische Substanz (wenn man deren
Polykondensate: Stärke und Zellulose, mit berücksichtigt).
weitere Informationen
 08/1998 - 12/1999 -
05/2001 - 09/2002 -
03/2005 - 02/2006 -
05/2009 - 10/2011
08/1998 - 12/1999 -
05/2001 - 09/2002 -
03/2005 - 02/2006 -
05/2009 - 10/2011
 zurück
zurück
Glycerin / Glycerol 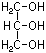 (C3H8O3)
(C3H8O3)
(Propantriol), farblose, ölige Flüssigkeit, Bestandteil der Fette.
R 36 - S 26
weitere Informationen
 06/1998 - 08/2002
- 07/2015
06/1998 - 08/2002
- 07/2015
 zurück
zurück
Glycin 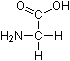 (C2H5NO2)
(C2H5NO2)
(a-Aminoessigsäure, Glykokoll), proteinogene Aminosäure.
Bildet farblose, gut wasserlösliche, süßlich schmeckende Kristalle.
Glycin besitzt, im Gegensatz zu allen anderen proteinogenen Aminosäuren, kein
Chiralitätszentrum, sie ist nicht optisch aktiv.
weitere Informationen
 09/2000 - 10/2001 -
06/2008 - 06/2009
09/2000 - 10/2001 -
06/2008 - 06/2009
 zurück
zurück
Harnsäure 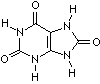 (C5H4N4O3)
(C5H4N4O3)
bildet farblose Kristalle, die in Wasser wenig löslich sind (ca. 75 mg/l), in Alkoholen und anderen
organischen Lösungsmitteln praktisch unlöslich, jedoch gut löslich in Laugen.
Abbauprodukt der Purine im menschlichen Organismus.
weitere Informationen
 07/2010
07/2010
 zurück
zurück
Harnstoff 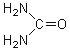 (CH4N2O)
(CH4N2O)
(Kohlensäurediamid), bildet farblose Kristalle, gut
wasserlöslich. Harnstoff entsteht im Säuger-Organismus beim Aminosäure-Abbau
(Harnstoffzyklus).
Die Harnstoff-Synthese durch Erhitzen von Ammoniumcyanat durch FRIEDRICH
WÖHLER (1828) gilt als Beginn der modernen organischen Chemie.
weitere Informationen
 02/1999 - 02/2005
- 10/2016
02/1999 - 02/2005
- 10/2016
 zurück
zurück
Hydrochinon 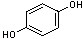 (C6H6O2)
(C6H6O2)
(1,4-Dihydroxybenzol), bildet farblose Nadeln, die in kaltem Wasser wenig, in heißem Wasser
gut löslich sind. Löslich in Alkohol, Ether und Benzol.
Hydrochinon wird vor allem als Reduktionsmittel in photographischen Entwicklerlösungen verwendet.
Es ist reizend und wassergefährdend, möglicherweise cancerogen.
R 22, 40/41/43, 50 - S 26, 36/37/39, 61
weitere Informationen
 12/2000
12/2000
 zurück
zurück
Indigocarmin 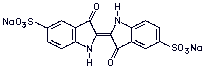 (C16H8N2Na2O8S2)
(C16H8N2Na2O8S2)
(Indigo-5,5'-disulfonsäure Natriumsalz) blauer, wasserlöslicher Farbstoff.
S 22, 24/25
weitere Informationen
 04/1998 - 06/1998 -
09/2002 - 01/2018
04/1998 - 06/1998 -
09/2002 - 01/2018
 zurück
zurück
Indikator
(lat.: indicare = anzeigen) Am Häufigsten werden Säure-Base-
und Redox-Indikatoren eingesetzt. Diese Substanzen sind je nach ihrem
Zustand (sauer/alkalisch bzw. oxidiert/reduziert) unterschiedlich
gefärbt.
Beispiele: Säure-Base-Indikatoren:
Bromthymolblau,
Kongorot,
Methylorange,
Methylrot,
Phenolphthalein,
Thymolblau.
Mischindikatoren (z.B. Universalindikator,
Tashiro-Mischindikator) enthalten verschiedene Substanzen.
Redox-Indikatoren: Ferroin,
Indigocarmin.
weitere Informationen
 zurück
zurück
Jod, I2
Blauschwarze Kristalle, ätzend, die Dämpfe wirken reizend.
R 20/21 - S 23, 25
weitere Informationen
 zurück
zurück
1-Jodbutan,  (C4H9J)
(C4H9J)
(n-Butyliodid), organisches Lösungsmittel, gesundheitsschädlich.
R 10, 20 - S 9, 29
 05/2007
05/2007
 zurück
zurück
Jodkaliumjodid-Lösung, KI·I2
(Jodjodkalium-Lösung), braune Flüssigkeit, die durch Auflösen
von elementarem Jod in einer
Kaliumjodid-Lösung hergestellt wird.
Es entsteht dabei das I3--Anion, bei höheren
Jodkonzentrationen größere Polyjodide. Durch diese Reaktion
kann erheblich mehr Jod gelöst werden als in reinem Wasser.
Jodkaliumjodid-Lösungen werden insbesondere in der Jodometrie verwendet,
sowie als Lugolsche Lösung in der Mikroskopie und zum
Stärke-Nachweis.
weitere Informationen
 08/1999 - 04/2000
- 03/2004 - 08/2007
- 02/2011 - 06/2011
- 10/2012 - 10/2019
- 02/2026
08/1999 - 04/2000
- 03/2004 - 08/2007
- 02/2011 - 06/2011
- 10/2012 - 10/2019
- 02/2026
 zurück
zurück
Kalilauge, KOH
Lösung von Kaliumhydroxid in Wasser. Ätzend.
R 35 -
S 26, 37/39, 45
weitere Informationen
 06/2002
06/2002
 zurück
zurück
Kaliumbromid, KBr
bildet farblose, gut wasserlösliche Kristalle.
weitere Informationen
 02/2010
02/2010
 zurück
zurück
Kaliumcarbonat, K2CO3
(Pottasche) Weißes, kristallines Pulver, gut wasserlöslich. In wasserfreiem Zustand hygroskopisch.
Gesundheitsschädlich, reizend.
R 22, 37/38 -
S 22, 28
weitere Informationen
 01/2001 - 02/2002
- 03/2015
01/2001 - 02/2002
- 03/2015
 zurück
zurück
Kaliumchlorat, KClO3
Farblose Kristalle, brandfördernd. Bei Kontakt mit brennbaren Stoffen
Explosionsgefahr!
R 9, 20/22 - S 2, 13, 16, 27
weitere Informationen
 12/1998 - 04/2006 -
07/2011
12/1998 - 04/2006 -
07/2011
 zurück
zurück
Kaliumchlorid, KCl
bildet farblose, gut wasserlösliche Kristalle; schmeckt stark salzig.
In der Natur kommt es als Sylvin (reines KCl) und Carnallit (Doppelsalz aus KCl+MgCl2) vor.
KCl wird als Düngemittel eingesetzt, KCl-Lösungen insbesondere als Elektrolyt-Lösungen,
z.B. für elektrochemische Zellen.
Kaliumchlorid ist oral ungiftig, bei Injektion einer KCl-Lösung kann Herzstillstand eintreten.
weitere Informationen
 09/2006
09/2006
 zurück
zurück
Kaliumchromat, K2CrO4
Gelbe Kristalle, wie alle Chromate ein starkes Oxidationsmittel.
Bei Kontakt mit brennbaren organischen Stoffen besteht Explosionsgefahr,
aus Salzsäure wird Chlorgas freigesetzt.
Brandfördernd, reizend, giftig, umweltschädigend und vermutlich cancerogen.
R 36/37/38, 43, 46, 49, 50 -
S 22, 28, 45, 53, 61
weitere Informationen
 01/2014
01/2014
 zurück
zurück
Kaliumdichromat, K2Cr2O7
Orangerote Kristalle, wie alle Chromate ein starkes Oxidationsmittel.
Bei Kontakt mit brennbaren organischen Stoffen besteht Explosionsgefahr,
aus Salzsäure wird Chlorgas freigesetzt.
Brandfördernd, reizend, giftig, umweltschädigend und vermutlich cancerogen.
R 36/37/38, 43, 46, 49, 50 -
S 22, 28, 45, 53, 61
weitere Informationen
 09/2001 - 02/2002
- 07/2002 - 07/2006
- 08/2019
09/2001 - 02/2002
- 07/2002 - 07/2006
- 08/2019
 zurück
zurück
Kaliumhexacyanoferrat(II) Trihydrat,
K4[Fe(CN)6] · 3 H2O
Gelbes Blutlaugensalz, bildet hellgelbe Kristalle.
Bei der Reaktion des Hexacyanoferrats(II) mit Fe3+-Ionen entsteht
ein tiefblauer Niederschlag, das "Berliner Blau".
R 32 - S 22, 24/25
weitere Informationen
 03/1999 - 10/1999 -
03/2001 - 01/2002 -
02/2014 - 08/2016 -
07/2017
03/1999 - 10/1999 -
03/2001 - 01/2002 -
02/2014 - 08/2016 -
07/2017
 zurück
zurück
Kaliumhexacyanoferrat(III), K3[Fe(CN)6]
Rotes Blutlaugensalz, leuchtendrote Kristalle. Zersetzt sich unter
Lichteinwirkung, besonders in wässriger Lösung, unter
HCN-Entwicklung. (giftig!)
R 32 - S 22, 24/25
weitere Informationen
 07/1998 - 01/2006
07/1998 - 01/2006
 zurück
zurück
Kaliumhydrogenphosphat, K2HPO4
bildet farblose, gut wasserlösliche Kristalle. In Alkohol praktisch unlöslich.
Die wässrige Lösung reagiert schwach alkalisch. Reizend.
R 36, 38 -
S 22, 24
 01/2010 - 07/2010
01/2010 - 07/2010
 zurück
zurück
Kaliumhydrogentartrat, KC4H5O6
(L(+)-Weinsäure-Monokaliumsalz, Weinstein) Schwerlösliches Salz der
Weinsäure. Weinstein kristallisiert, meist zusammen mit
Calciumtartrat, aus dem vergorenen Wein aus und bildet an den Wänden der Weinfässer
oft dicke Krusten. Er kann sich auch noch nach dem Abfüllen in der Flasche bilden,
was als Qualitätsmerkmal gilt.
weitere Informationen
 01/2001
01/2001
 zurück
zurück
Kaliumhydroxid, KOH
Ätzkali, kommt meist als weiße
Plätzchen in den Handel. Stark ätzend und hygroskopisch.
R 35 -
S 26, 37/39, 45
weitere Informationen
 02/2003
02/2003
 zurück
zurück
Kaliumjodat, KIO3
Farblose Kristalle, reizend, gesundheitsschädlich. Wird in kleinen
Mengen dem ("jodierten") Speisesalz beigegeben.
R 9 - S 17, 22, 24/25
weitere Informationen
 12/1998 - 04/2008 -
08/2008
12/1998 - 04/2008 -
08/2008
 zurück
zurück
Kaliumjodid, KI
Bildet farblose, würfelförmige Kristalle. In Wasser, Methanol, Ethanol und
Glycerin (relativ) gut löslich. Bei Feststoff und Lösung tritt
bei längerem Luftkontakt infolge Oxidation eine leichte Gelbfärbung
auf. (Jod-Freisetzung) Für jodiertes Speisesalz wird heute - aufgrund der
besseren Stabilität - meist Kaliumjodat verwendet.
weitere Informationen
 09/2005 - 04/2008 -
07/2011 - 02/2016
- 02/2018
09/2005 - 04/2008 -
07/2011 - 02/2016
- 02/2018
 zurück
zurück
Kaliumnatriumtartrat Tetrahydrat, KNaC4H4O6 · 4 H2O
(Seignettesalz, Natronweinstein) Gemischtes Salz der Weinsäure, bildet
farblose, gut wasserlösliche Kristalle. Die Kristalle zeigen piezoelektrische Eigenschaften.
Tartrate wirken als Reduktionsmittel, Seignettesalz kommt daher unter anderem bei der Versilberung
von Spiegeln zum Einsatz.
Kaliumnatriumtartrat wurde um 1650 von dem französischen Apotheker SEIGNETTE
durch Neutralisation von Kaliumhydrogentartat (Weinstein) mit
Natriumcarbonat (Soda) hergestellt.
weitere Informationen
 04/2000 - 03/2005 -
11/2007 - 12/2009 -
11/2010
04/2000 - 03/2005 -
11/2007 - 12/2009 -
11/2010
 zurück
zurück
Kaliumnitrat, KNO3
(Salpeter) Farblose Kristalle, gut wasserlöslich. Brandfördernd.
R 7 -
S 17
weitere Informationen
 02/1999 - 07/2007
- 12/2013 - 08/2025
02/1999 - 07/2007
- 12/2013 - 08/2025
 zurück
zurück
Kaliumoxalat, K2C2O4
Farblose Kristalle, gut wasserlöslich. Gesundheitsschädlich.
R 21/22 -
S 24/25
weitere Informationen
 08/2019
08/2019
 zurück
zurück
Kaliumpermanganat, KMnO4
"Übermangansaures Kali", dunkelviolette Kristalle, gut wasserlöslich.
Oxidiert organisches Material unter Abscheidung von Braunstein, brandfördernd,
gesundheitsschädlich.
R 8, 22 -
S 22, 24/25
weitere Informationen
 11/1998 - 02/1999 -
07/1999 - 10/1999 -
08/2002 - 06/2003 -
02/2004 - 04/2004 -
04/2005 - 06/2014
11/1998 - 02/1999 -
07/1999 - 10/1999 -
08/2002 - 06/2003 -
02/2004 - 04/2004 -
04/2005 - 06/2014
 zurück
zurück
Kaliumphosphat, K3PO4
Kaliumsalz der Phosphorsäure, bildet ein weißes, hygroskopisches Pulver,
das gut in Wasser löslich ist (90g/100ml). In Alkoholen unlöslich.
Eine wässrige Lösung reagiert stark alkalisch. Reizend.
R 38 -
S 26, 28
weitere Informationen
 01/2003 - 02/2010
01/2003 - 02/2010
 zurück
zurück
Kaliumthiocyanat, KSCN
(Kaliumrhodanid), bildet farblose, hygroskopische, gut wasserlösliche Kristalle.
Kaliumthiocyanat wird durch Zusammenschmelzen von Kaliumcyanid und Schwefel oder durch
Umsetzung von Ammoniumthiocyanat mit Kaliumhydroxid hergestellt. Verwendung unter anderem
als Komplexbildner für Fe3+-Ionen (charakteristische tiefrote Färbung),
in der organischen Synthese, als Komponente von Metallbeizen, Druckfarben usw..
Gesundheitsschädlich.
R 22 -
S 22, 24/25
weitere Informationen
 03/1999 - 10/1999 -
02/2001 - 01/2002 -
10/2011 - 01/2016
03/1999 - 10/1999 -
02/2001 - 01/2002 -
10/2011 - 01/2016
 zurück
zurück
Kobalt(II)chlorid Hexahydrat, CoCl2 · 6 H2O
Tiefrote Kristalle, giftig. Ab 35°C beginnt unter Abgabe von Kristallwasser die
Umwandlung in das dunkelblaue, wasserfreie CoCl2.
R 23/24/25 -
S 22, 24/25, 53
weitere Informationen
 03/1998 - 10/2000 -
09/2004 - 10/2007
03/1998 - 10/2000 -
09/2004 - 10/2007
 zurück
zurück
Kongorot 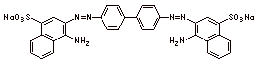 (C32H22N6Na2O6S2)
(C32H22N6Na2O6S2)
Säure-Base-Indikator (pH 3,0-5,2: blau 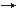 rot);
wurde als substantiver Farbstoff in der Färberei (für Baumwolle und andere
Cellulose-Fasern) eingesetzt, aufgrund des Verdachts auf cancerogene Wirkung aber
inzwischen durch unbedenkliche Farbstoffe ersetzt. Es wird aber noch in der Mikroskopie
eingesetzt. Kongorot ist möglicherweise cancerogen, daher Hautkontakt vermeiden.
R 45, 63 - S 45, 53
rot);
wurde als substantiver Farbstoff in der Färberei (für Baumwolle und andere
Cellulose-Fasern) eingesetzt, aufgrund des Verdachts auf cancerogene Wirkung aber
inzwischen durch unbedenkliche Farbstoffe ersetzt. Es wird aber noch in der Mikroskopie
eingesetzt. Kongorot ist möglicherweise cancerogen, daher Hautkontakt vermeiden.
R 45, 63 - S 45, 53
weitere Informationen
 04/1998 - 07/2005
04/1998 - 07/2005
 zurück
zurück
Kristallviolett 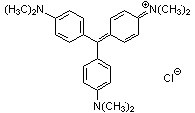 (C25H30N3Cl)
(C25H30N3Cl)
Sehr gut wasserlöslicher Triphenylmethanfarbstoff. Gesundheitsschädlich, kann insbesondere Augenschäden verursachen!
R 22, 40/41, 50/53 - S 26, 36/37/39, 46, 60/61
weitere Informationen
 07/2009
07/2009
 zurück
zurück
Kupfer, Cu
Rötliches Edelmetall mit hoher thermischer und elektrischer
Leitfähigkeit. Bildet den Hauptbestandteil von Messing (Legierung
mit Zink) und Bronze (Legierung mit Zinn).
weitere Informationen
 07/1998 - 05/2000 -
09/2003 - 06/2006 -
08/2009 - 04/2014
07/1998 - 05/2000 -
09/2003 - 06/2006 -
08/2009 - 04/2014
 zurück
zurück
Kupfer(II)acetat Monohydrat, Cu(CH3COO)2 · H2O
Dunkelblaugrüne Kristalle, die in Wasser, Methanol und Ethanol gut löslich sind.
Gesundheitsschädlich.
R 20/22 -
S 28
weitere Informationen
 12/2025
12/2025
 zurück
zurück
Kupfer(II)chlorid Dihydrat, CuCl2 · 2 H2O
Blaugrüne Kristalle, die in Wasser, Methanol und Ethanol gut, in anderen
organischen Lösungsmitteln wenig oder nicht löslich sind.
Konzentrierte wässrige Lösungen sind braun, verdünnte Lösungen
grün 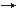 blau;
sie reagieren schwach sauer. Gesundheitsschädlich.
R 20/22 -
S 28
blau;
sie reagieren schwach sauer. Gesundheitsschädlich.
R 20/22 -
S 28
weitere Informationen
 05/2003 - 12/2003
- 08/2004
05/2003 - 12/2003
- 08/2004
 zurück
zurück
Kupfer(II)nitrat Trihydrat, Cu(NO3)2 · 3 H2O
bildet dunkelblaue, sehr gut wasserlösliche, hygroskopische Kristalle.
Beim Erhitzen wird Wasser und Salpetersäure abgegeben, bei höheren Temperaturen
(> 170°C) zerfällt das Salz in CuO, NO und O2.
Brandfördernd, reizend.
R 8, 38 -
S 28
weitere Informationen
 07/2007
07/2007
 zurück
zurück
Kupfer(II)sulfat Pentahydrat, CuSO4 · 5 H2O
(Kupfervitriol) bildet tiefblaue Kristalle, die in Wasser gut, in organischen
Lösungsmitteln nicht löslich sind. In der Natur kommt Kupfersulfat als
Verwitterungsprodukt sulfidischer Kupfererze als krustenförmige, körnige
oder faserige Aggregate vor. (Chalkanthit) Technisch wird Kupfersulfat
durch Einwirkung von Schwefelsäure auf Kupferoxide oder -sulfide gewonnen.
Es ist das mit Abstand wichtigste Kupfersalz. Gesundheitsschädlich.
R 22, 37/38 -
S 22, 28
weitere Informationen
 02/1998 - 06/2000 -
08/2000 - 03/2001 -
04/2001 - 10/2001 -
02/2002 - 10/2003 -
12/2003 - 01/2005 -
03/2005 - 11/2007 -
12/2009 - 11/2010 -
03/2011 - 06/2013 -
02/2014 - 12/2017 -
08/2023 - 08/2024 -
06/2025 - 08/2025
02/1998 - 06/2000 -
08/2000 - 03/2001 -
04/2001 - 10/2001 -
02/2002 - 10/2003 -
12/2003 - 01/2005 -
03/2005 - 11/2007 -
12/2009 - 11/2010 -
03/2011 - 06/2013 -
02/2014 - 12/2017 -
08/2023 - 08/2024 -
06/2025 - 08/2025
 zurück
zurück
Lebertran
Oleum Jecoris, aus Fischleber gewonnenes gelbes Öl.
weitere Informationen
 06/1998 - 01/2012
06/1998 - 01/2012
 zurück
zurück
Leichtbenzin / Ligroin  Benzin
Benzin
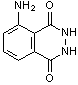 (C8H7N3O2)
(C8H7N3O2) 01/2006 - 05/2016
01/2006 - 05/2016 zurück
zurück
Magnesium, Mg
Erdalkalimetall. Wird von Wasser nur langsam, von Säuren sehr leicht angegriffen.
Beim Entzünden von Magnesiumband oder Pulver verbrennt es an der Luft mit
grellweißer Flamme. Deshalb wurde es früher als "Blitzlicht-Pulver"
verwendet.
weitere Informationen
 02/2000
02/2000
 zurück
zurück
Magnesiumbromid, MgBr2
bildet farblose, hygroskopische, gut wasserlösliche Kristalle.
MgBr2 entsteht als Nebenprodukt bei GRIGNARD-Reaktionen. Reizend.
R 36/37/38 - S 36, 36
weitere Informationen
 01/2008
01/2008
 zurück
zurück
Magnesiumchlorid, MgCl2
bildet als Hexahydrat farblose, hygroskopische Kristalle, die durch hydrolytische HCl-Freisetzung
stark korrodierend und reizend wirken.
In der Natur kommt es gelöst sowie als Carnallit (Doppelsalz aus KCl+MgCl2) vor.
R 36/37 - S 36
weitere Informationen
 02/2010 - 07/2010
- 12/2014
02/2010 - 07/2010
- 12/2014
 zurück
zurück
Malonsäure 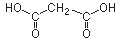 (C3H4O4)
(C3H4O4)
(Propandisäure), farblose Kristalle, gut wasserlöslich, reizend, gesundheitsschädlich.
R 22, 37/38 - S 22, 26, 28
weitere Informationen
 05/1998 - 08/2008
05/1998 - 08/2008
 zurück
zurück
Mangan(II)chlorid, MnCl2·4H2O
rosafarbene Kristalle, sehr gut wasserlöslich;
gesundheitsschädlich, umweltgefährlich.
R 20/22, 48, 51/53 - S 22, 61
weitere Informationen
 09/2024
09/2024
 zurück
zurück
Mangan(IV)oxid, MnO2
(Braunstein) braunschwarzes Pulver; in Wasser und Säuren nahezu unlöslich.
gesundheitsschädlich, umweltgefährlich.
R 20/22 - S 25
weitere Informationen
 07/2023
07/2023
 zurück
zurück
Mangansulfat, MnSO4·H2O
schwach rosafarbenes, gut wasserlösliches Pulver;
gesundheitsschädlich, umweltgefährlich.
R 20/22, 48, 51/53 - S 22, 61
weitere Informationen
 08/2008 - 05/2014
08/2008 - 05/2014
 zurück
zurück
Methanol, CH3OH
(Methylalkohol), giftig, leichtentzündlich.
R 11, 23/25 - S 7, 16, 24, 45
weitere Informationen
 06/1998 - 02/2002 -
01/2004 - 12/2005 -
09/2007 - 04/2009 -
12/2022 - 02/2026
06/1998 - 02/2002 -
01/2004 - 12/2005 -
09/2007 - 04/2009 -
12/2022 - 02/2026
 zurück
zurück
Methylenblau 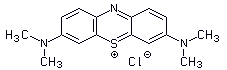 (C16H18ClN3S
· aq)
(C16H18ClN3S
· aq)
Blauer wasserlöslicher Farbstoff, wird vor allem in der Mikroskopie eingesetzt,
gesundheitsschädlich.
Komponente des Tashiro-Mischindikators.
R 22 - S 22, 24/25
weitere Informationen
 06/1998 - 08/1998 -
01/1999 - 06/2001 -
02/2008 - 02/2017
06/1998 - 08/1998 -
01/1999 - 06/2001 -
02/2008 - 02/2017
 zurück
zurück
Methylorange 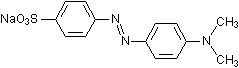 (C14H14N3NaO3S)
(C14H14N3NaO3S)
(4-[4-(Dimethylamino)phenylazo]benzolsulfonsäure-Natriumsalz), orangegelbes, wasserlösliches
Pulver. In Alkohol kaum löslich. Giftig.
Säure-Base-Indikator: pH 3,0-4,4 (rot 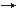 gelb)
R 25 - S 36/37/38, 45
gelb)
R 25 - S 36/37/38, 45
weitere Informationen
 11/2000 - 06/2001 -
02/2002 - 08/2017
11/2000 - 06/2001 -
02/2002 - 08/2017
 zurück
zurück
Methylrot 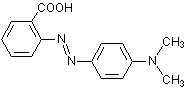 (C15H15N3O2)
(C15H15N3O2)
(2-[4-(Dimethylamino)phenylazo]-benzoesäure) Bildet violette Nadeln, die in Wasser kaum,
in Alkohol und Essigsäure gut löslich sind.
Säure-Base-Indikator: pH 4,4-6,2 (rot 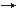 gelb),
Komponente des Tashiro-Mischindikators.
S 36/37/38, 45
gelb),
Komponente des Tashiro-Mischindikators.
S 36/37/38, 45
weitere Informationen
 11/2000 - 06/2001 -
02/2002 - 03/2003
11/2000 - 06/2001 -
02/2002 - 03/2003
 zurück
zurück
α-Naphthol 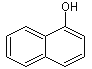 (C10H8O)
(C10H8O)
(1-Naphthol). Farblose Kristalle mit phenolischem Geruch. In Wasser kaum, in
organischen Lösungsmitteln und Alkalilaugen gut löslich.
Unter Lichteinwirkung färbt sich 1-Naphthol dunkel.
Hautschädigend, stark reizend, gesundheitsschädlich.
R 21, 36/38, 41, 42/43 - S 22, 26, 36/37/38
 02/2005
02/2005
 zurück
zurück
β-Naphthol 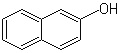 (C10H8O)
(C10H8O)
(2-Naphthol). Farblose Kristalle, die in kaltem Wasser kaum, in warmem Wasser etwas
löslich sind. In organischen Lösungsmitteln und Alkalilaugen
gut löslich. Hautschädigend, mindergiftig.
R 20/22 - S 24/25
 04/1999
04/1999
 zurück
zurück
α-Naphthylamin 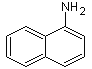 (C10H9N)
(C10H9N)
(1-Amino-naphthalin), bildet farblose Nadeln mit unangenehmem Geruch.
In Wasser praktisch unlöslich, in organischen Lösungsmitteln gut
löslich. Giftig, möglicherweise cancerogen, umweltgefährdend.
R 22, 45, 51/53 -
S 24, 45, 53, 61
 04/1999 - 12/2013
04/1999 - 12/2013
 zurück
zurück
Natriumacetat Trihydrat, CH3COONa·3H2O
Natriumsalz der Essigsäure, bildet farblos durchscheinende,
gut wasserlösliche Kristalle (170g/100ml). In Ethanol löslich (ca. 5g/100ml).
Eine wässrige Lösung reagiert alkalisch.
weitere Informationen
 01/2003 - 02/2009
01/2003 - 02/2009
 zurück
zurück
Natriumbromat, NaBrO3
Farblose Kristalle, reizend, brandfördernd.
R 8, 22, 36/37/38 - S 17, 26, 36
weitere Informationen
 05/1998 - 02/2016
05/1998 - 02/2016
 zurück
zurück
Natriumbromid, NaBr
Farblose Kristalle, reizend.
R 36/37/38 - S 26, 36
weitere Informationen
 05/1998 - 02/2016
05/1998 - 02/2016
 zurück
zurück
Natriumcarbonat, Na2CO3
(Soda) Wasserfreies Natriumcarbonat bildet ein weißes, Haut und Schleimhäute
reizendes Pulver. Daneben existieren drei Hydrate: Monohydrat, Heptahydrat und Decahydrat.
Alle drei Hydrate bilden farblose Kristalle. Natriumcarbonat-Lösungen reagieren stark
alkalisch. Reizend.
R 36 - S 22, 26
weitere Informationen
 11/2000 - 01/2003 -
07/2005 - 10/2009 -
03/2012 - 04/2013 -
12/2015
11/2000 - 01/2003 -
07/2005 - 10/2009 -
03/2012 - 04/2013 -
12/2015
 zurück
zurück
Natriumchlorid, NaCl
Kochsalz, Steinsalz, farblose Kristalle, in Wasser gut, in Alkoholen
kaum löslich.
Eine 0,9%ige Kochsalzlösung hat den gleichen osmotischen Druck wie das Blutplasma.
Sie kommt als isotonische Kochsalzlösung bei intravenösen Injektionen und
Infusionen zum Einsatz.
weitere Informationen
 07/1998 - 04/1999 -
07/2000 - 07/2005 -
09/2005 - 09/2011 -
01/2013 - 10/2016
07/1998 - 04/1999 -
07/2000 - 07/2005 -
09/2005 - 09/2011 -
01/2013 - 10/2016
 zurück
zurück
Natriumcitrat Dihydrat, Na3C6H5O7 · 2 H2O
Natriumsalz der Zitronensäure, bildet
farblose, wasserlösliche Kristalle. Die wässrige Lösung reagiert stark alkalisch.
 01/2010
01/2010
 zurück
zurück
Natriumdithionit, Na2S2O4
(Natriumhyposulfit) Weißes, gut wasserlösliches Pulver.
Dithionit wird durch Reduktion von Sulfit gewonnen. Diese Reaktion ist reversibel,
daher ist Natriumdithionit ein starkes Reduktionsmittel, das in der Färberei
(vor allem in der Küpenfärberei), zum Bleichen von Zucker, Sirup und
holzhaltigem Papier sowie zur Silber-Reduktion aus Fixierbädern verwendet wird. Reizend.
R 22, 31, 37 - S 7/8, 26, 28, 43
weitere Informationen
 08/2001 - 03/2010
- 12/2011 - 12/2012
- 01/2018 - 03/2024
08/2001 - 03/2010
- 12/2011 - 12/2012
- 01/2018 - 03/2024
 zurück
zurück
Natriumformiat, HCOONa
Natriumsalz der Ameisensäure, farbloses
Pulver, gut wasserlöslich. Reizend.
R 36/37/38 - S 26, 36
weitere Informationen
 11/1998
11/1998
 zurück
zurück
Natriumhydrogencarbonat, NaHCO3
(Natron, Natriumbicarbonat) Weißes, gut wasserlösliches, alkalisch
schmeckendes Pulver. Wässrige Lösungen reagieren schwach alkalisch.
Beim Erwärmen (über 50°C) Umwandlung zu Na2CO3
unter Abspaltung von CO2 und H2O.
Bestandteil von Brausepulver, Backpulver und Antazida.
S 22, 24/25
weitere Informationen
 05/2005
05/2005
 zurück
zurück
Natriumhydrogensulfat Monohydrat, NaHSO4·H2O
Mono-Natriumsalz der Schwefelsäure; bildet farblose, gut
wasserlösliche Kristalle. Hydrogensulfate reagieren in Lösung stark sauer.
Ätzend.
Beim Erhitzen wird zunächst das Kristallwasser abgegeben, ab 460°C
erfolgt unter Wasserabspaltung eine Umwandlung zu Natriumdisulfat.
R 34, 37 - S 26, 36/37/39, 45
weitere Informationen
 11/2000 - 01/2003
11/2000 - 01/2003
 zurück
zurück
Natriumhydrogensulfit, NaHSO3
Mono-Natriumsalz der schwefligen Säure, farblose Kristalle, reizend.
R 22, 36/38, 40 - S 26, 36/37
weitere Informationen
 12/1998 - 01/2002
12/1998 - 01/2002
 zurück
zurück
Natriumhydroxid, NaOH
Ätznatron, "kaustisches Soda", kommt meist als weiße
Plätzchen in den Handel. Stark ätzend und hygroskopisch.
R 35 -
S 26, 37/39, 45
weitere Informationen
 08/1998 - 09/2002 -
03/2005 - 06/2025
08/1998 - 09/2002 -
03/2005 - 06/2025
 zurück
zurück
Natriumnitrit, NaNO2
Natriumsalz der salpetrigen Säure. Bildet farblose, gut wasserlösliche
Kristalle. Bestandteil des Pökelsalzes. Giftig, brandfördernd.
R 8, 25 - S 45
weitere Informationen
 04/1999 - 02/2005
04/1999 - 02/2005
 zurück
zurück
Natriumperoxid, Na2O2
Peroxid des Natriums. Bildet ein gelbliches, hygroskopisches Pulver.
Natriumperoxid wird in der Industrie als Oxidations- und Bleichmittel verwendet. Ätzend, brandfördernd.
R 8, 35 - S 8, 27, 39, 45
weitere Informationen
 05/2016
05/2016
 zurück
zurück
Natriumsilikat, Na[SiO3]
Natriumsalze polymerer Silikate; ätzend.
Kommen überwiegend als wässrige Lösungen = Natronwasserglas in den Handel.
R 38, 41 - S 26, 28, 37/39
weitere Informationen
 08/2011
08/2011
 zurück
zurück
Natriumsulfat Decahydrat, Na2SO4·10H2O
(Glaubersalz), Natriumsalz der Schwefelsäure; bildet farblose,
gut wasserlösliche Kristalle (50g/100ml). Oberhalb von 33°C wird das Kristallwasser
abgegeben, es entsteht wasserfreies Na2SO4 (Thenardit), das als
Trockenmittel für organische Lösungsmittel eingesetzt werden kann.
weitere Informationen
 01/2003 - 12/2014
01/2003 - 12/2014
 zurück
zurück
Natriumsulfit, Na2SO3
Natriumsalz der schwefligen Säure, farblose Kristalle, reizend.
R 22, 36/38, 40 - S 26, 36/37
weitere Informationen
 11/1998 - 12/1998 -
04/2005 - 10/2005 -
06/2014 - 07/2017 -
12/2017 - 03/2024
11/1998 - 12/1998 -
04/2005 - 10/2005 -
06/2014 - 07/2017 -
12/2017 - 03/2024
 zurück
zurück
Natriumtetraborat, Na2B4O7
(Borax) bildet farblose Kristalle, die in Wasser löslich sind.
Beim Erhitzen löst sich das Salz in seinem Kristallwasser, gibt bei höheren Temperaturen das Wasser weitgehend ab und bildet eine glasartige Schmelze.
In der Analytik nutzt man "Borax-Perlen" als Vorproben auf bestimmt Schwermetalle, da sich deren Salze mit charakteristischer Farbe darin lösen.
gesundheitsschädlich, möglicherweise teratogen!
R 21/22, 36/37/38 -
S 26, 36/37
weitere Informationen
 06/2022
06/2022
 zurück
zurück
Natriumthiosulfat, Na2S2O3 · 5 H2O
(Fixiersalz), Natriumsalz der Thioschwefelsäure, farblose Kristalle.
In der Fotografie wird Natriumthiosulfat zum "Fixieren" der Filme bzw.
Abzüge verwendet: Thiosulfat bildet mit Ag+-Ionen einen
stabilen Komplex, das nicht belichtete AgBr wird aus der lichtempfindlichen
Schicht herausgelöst. Somit wird ein Nachdunkeln der Fotografien
verhindert.
S 22, 24/25
weitere Informationen
 09/1999 -
08/2000 - 06/2005 -
08/2007 - 05/2008
09/1999 -
08/2000 - 06/2005 -
08/2007 - 05/2008
 zurück
zurück
Natriumwolframat Dihydrat, NaWO4 · 2 H2O
bildet farblose, gut wasserlösliche Kristalle.
Reizend.
R 36/37/38 -
S 26, 36
 08/2006
08/2006
 zurück
zurück
Natronlauge, NaOH
Lösung von Natriumhydroxid in Wasser. Ätzend.
R 35 -
S 26, 37/39, 45
weitere Informationen
 11/1998 - 04/1999 -
07/1999 - 10/1999 -
10/2001 - 05/2002 -
03/2003 - 10/2005 -
01/2006 - 07/2009 -
05/2010 - 07/2010 -
12/2010 - 03/2011 -
09/2012 - 11/2012 -
12/2012 - 01/2015 -
04/2016
11/1998 - 04/1999 -
07/1999 - 10/1999 -
10/2001 - 05/2002 -
03/2003 - 10/2005 -
01/2006 - 07/2009 -
05/2010 - 07/2010 -
12/2010 - 03/2011 -
09/2012 - 11/2012 -
12/2012 - 01/2015 -
04/2016
 zurück
zurück
Nickel(II)acetat Tetrahydrat, Ni(CH3COO)2 · 4 H2O
Grünes Salz, gut wasserlöslich, giftig.
R 43, 49 -
S 36/37/39, 45, 53
 06/1999
06/1999
 zurück
zurück
Nickel(II)chlorid Hexahydrat, NiCl2 · 6 H2O
Hellgrünes Salz, gut wasserlöslich, giftig.
R 25, 43, 49 -
S 36/37/39, 45, 53
weitere Informationen
 06/1999
06/1999
 zurück
zurück
Ninhydrin 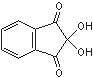 (C9H6O4)
(C9H6O4)
Ninhydrin bildet hellgelbe, gut wasserlösliche Kristalle. Es wird vor allem zum Nachweis
von Aminosäuren und Peptiden verwendet, mit denen es einen blauvioletten Farbstoff ergibt.
S 22, 24/25
weitere Informationen
 09/2000 - 06/2008
- 11/2017
09/2000 - 06/2008
- 11/2017
 zurück
zurück
Nitroprussidnatrium, Na2[Fe(CN)5(NO)]·2H2O
Natrium-Pentacyanonitrosylferrat(III) Dihydrat, orangerote Kristalle.
Einsatz in der Medizin zur Blutdrucksenkung (Freisetzung von NO, wirkt vasodilatierend = gefäßerweiternd),
in der anorganischen und organischen Analytik (Nachweis u.a. von Sulfiden, Thiolen und Ketonen) und zu Nachweis
von Ketonkörpern im Urin (Teststreifen).
R 20/21, 25 - S 9, 28, 36/37/39, 45
weitere Informationen
 05/2001 - 09/2012
- 04/2013 - 07/2017
05/2001 - 09/2012
- 04/2013 - 07/2017
 zurück
zurück
Oelsäure  (C18H34O2)
(C18H34O2)
Ölsäure (oleinsäure, cis-9-Octadecensäure) ist häufigste der einfach
ungesättigten Fettsäuren und kommt in fast allen pflanzlichen und tierischen Fetten vor.
Sie ist farblos, bei Raumtemperatur flüssig (Smp.: 17°C), in Wasser praktisch unlöslich aber
in fast allen organischen Lösungsmitteln gut löslich.
weitere Informationen
 03/2014
03/2014
 zurück
zurück
Orange II 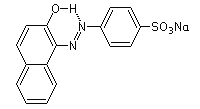 (C16H11N2NaO4S) · 5 H2O
(C16H11N2NaO4S) · 5 H2O
(ß-Naphtholorange, Säureorange A,
2-Hydroxy-naphthalin-1-azo-4'-benzolsulfonsäure Natriumsalz).
Rotbrauner Feststoff, gelöst leuchtend orange. Viel verwendeter
Textil-Farbstoff. Säure-Base-Indikator (pH 10,2...11,8: orange
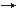 rot), Farbstoff für die Mikroskopie.
rot), Farbstoff für die Mikroskopie.
weitere Informationen
 04/1999
04/1999
 zurück
zurück
Oxalsäure 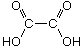 (C2H2O4)
(C2H2O4)
Oxalsäure bildet farblose Kristalle, die in Wasser und Ethanol
löslich sind. Wässrige Lösung reagieren stark sauer:
pKS1 = 1,27; pKS2 = 4,27.
Sie kommt in vielen Pflanzen vor, besonders in Sauerklee,
Rhabarber und Sauerampfer. Oxalsäure ist gesundheitsschädlich.
R 21/22 -
S 2, 24/25
weitere Informationen
 12/2002 - 06/2003
- 09/2006 - 12/2007
- 10/2008 - 03/2009
- 08/2019
12/2002 - 06/2003
- 09/2006 - 12/2007
- 10/2008 - 03/2009
- 08/2019
 zurück
zurück
Paraffin
Als Paraffin bezeichnet man Alkan-Gemische (also Gemische
gesättigter aliphatischer Kohlenwasserstoffe).
Sie sind mit Ether und Chloroform beliebig mischbar bzw.
löslich, in Wasser unlöslich. Außerdem dürfen
sie nicht fluoreszieren (d.h. sie müssen frei von aromatischen
Verbindungen sein). Sie können bei Raumtemperatur flüssig
oder fest sein. Nach ihrem Schmelzbereich und der Viskosität
unterscheidet man Paraffinöl (Weißöl), Weichparaffin,
Petrolatum (Vaseline) und Hartparaffin. Paraffine sind wenig reaktiv
(beständig gegen Schwefelsäure, Brom und kalte Salpetersäure).
Je nach Eigenschaften werden sie für Kosmetika, als Pflegemittel
(für Holz, Metall, Autolack usw.), Modelliermasse, zur Wachsung
von Lebensmitteln (Obst, Käse) oder für Kerzen verwendet.
Entzündlich oder brennbar.
R 10 -
S 16
weitere Informationen
 09/2003
09/2003
 zurück
zurück
1-Pentanol  (C5H12O)
(C5H12O)
(n-Amylalkohol) Farblose Flüssigkeit mit charakteristischem Geruch.
Hauptkomponente in Amylkohol. Mit Wasser wenig, mit
organischen Lösungsmitteln gut mischbar.
Pentanole wurden früher aus Fuselölen gewonnen, heute erfolgt die
Synthese meist durch Hydroformylierung von 1-Buten oder Hydrolyse von 1-Chlorpentan.
Entzündlich, reizend.
R 10, 20 -
S 24/25
weitere Informationen
 zurück
zurück
Petrolether  Benzin
Benzin
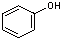 (C6H6O)
(C6H6O) 01/2004 - 09/2007
01/2004 - 09/2007 zurück
zurück
Phenolphthalein 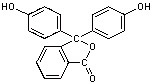 (C20H14O4)
(C20H14O4)
Weißes, geruchloses Pulver; in Alkohol und Alkalien löslich, in Wasser praktisch
unlöslich. Verwendung als Säure-Base-Indikator (pH 8,2-10,0: farblos 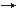 rot)
rot)
weitere Informationen
 08/1998 - 10/1999
- 06/2001 - 03/2003
- 12/2010 - 08/2012
- 01/2015
08/1998 - 10/1999
- 06/2001 - 03/2003
- 12/2010 - 08/2012
- 01/2015
 zurück
zurück
Phosphorsäure, H3PO4
Anorganische Säure, bildet als Reinstoff farblose Kristalle (Schmelzpunkt: 42,4°C; bildet oft unterkühlte
Schmelzen); im Handel ist vorwiegend eine 85%ige Lösung. Ätzend.
R 34 - S 26, 45
weitere Informationen
 03/2013 - 05/2014 -
03/2025
03/2013 - 05/2014 -
03/2025
 zurück
zurück
Phthalsäureanhydrid 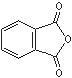 (C8H4O3)
(C8H4O3)
Farblose, kaum wasserlösliche Substanz; kommt meist in Form weißer Blättchen
in den Handel. Mit Alkoholen bilden sich beim Erwärmen die Ester.
Phthalsäureanhydrid dient in erster Linie als Ausgangssubstanz für
Phthalein-Farbstoffe und Alkydharzen (verzweigtkettige Polyester aus Dicarbonsäuren
und drei- und höherwertigen Alkoholen, z.B. Glycerin). Reizend.
R 36/37/38 -
S 22, 24/25
weitere Informationen
 12/2004
12/2004
 zurück
zurück
L-Prolin 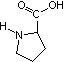 (C5H9NO2)
(C5H9NO2)
(S-Pyrrolidin-2-carbonsäure), proteinogene, nicht essentielle Aminosäure.
Bildet farblose, gut wasserlösliche Kristalle. Optisch aktiv.
weitere Informationen
 09/2000
09/2000
 zurück
zurück
1-Propanol, 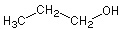 (C3H8O)
(C3H8O)
(n-Propanol, Propylalkohol) Farblose Flüssigkeit,
mit Wasser und den meisten organischen Lösungsmitteln mischbar.
n-Propanol ist als Nebenprodukt der alkoholischen Gärung Bestandteil
der Fuselöle. Es wird hauptsächlich als Lösungsmittel eingesetzt,
insbesondere für kosmetische Präparate und Desinfektionsmittel,
denn es besitzt eine stärker bakterizide Wirkung als Ethanol.
Leichtentzündlich.
R 11 -
S 7, 16
weitere Informationen
 07/1999
07/1999
 zurück
zurück
2-Propanol, 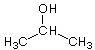 (C3H8O)
(C3H8O)
(Isopropylalkohol, "Isopropanol") Organisches Lösungsmittel,
mit Wasser und vielen anderen organischen Lösungsmitteln gut
mischbar. 2-Propanol wird zur Estersynthese, zur Darstellung von Aceton
(durch Oxidation) und für Frostschutz- und Enteisungsmittel verwendet.
In erster Linie dient es jedoch als Lösungsmittel für Kunst-
und Naturharze sowie - da es auch Fette und Proteine gut löst - in
Reinigungsmitteln. Leichtentzündlich.
R 11 -
S 7, 16
weitere Informationen
 03/1998 - 07/1999 -
04/2002 - 05/2004 -
09/2010
03/1998 - 07/1999 -
04/2002 - 05/2004 -
09/2010
 zurück
zurück
Propionsäure, 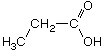 , (C3H6O2)
, (C3H6O2)
(Propansäure) Farblose Flüssigkeit mit unangenehmem Geruch. Ätzend.
R 35 -
S 2, 23, 26
weitere Informationen
 05/2025
05/2025
 zurück
zurück
Quecksilberchlorid, HgCl2
Weißes, wenig lösliches Salz. Hochgiftig, ätzend.
R 28, 34, 48/24/25 -
S 36/37/39, 45
weitere Informationen
 10/1998 - 12/1998
10/1998 - 12/1998
 zurück
zurück
Resorcin 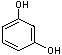 (C6H6O2)
(C6H6O2)
(1,3-Dihydroxybenzol) Farblose, sehr gut wasserlösliche Substanz;
bildet farblose/durchscheinende Kristalle. Wässrige Lösungen reagieren
schwach sauer. (pKS1=9,15; pKS2=11,32)
Gut löslich in Alkoholen und Diethylether, in Benzol und Chloroform
kaum löslich. An der Luft färbt sich die Substanz allmählich rosa.
Resorcin wird zur Herstellung vieler Phenoplaste, Farbstoffe und synthetischer
Gerbstoffe benötigt. Gesundheitsschädlich und reizend.
R 22, 36/38 -
S 26
weitere Informationen
 12/2004 - 02/2006 -
09/2007 - 03/2009
12/2004 - 02/2006 -
09/2007 - 03/2009
 zurück
zurück
Rhodamin B 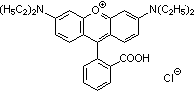 (C28H31ClN2O3)
(C28H31ClN2O3)
rotviolettes kristallines Pulver, gut löslich in Wasser unter Bildung einer intensiv
blauvioletten Lösung. Rhodamin B wird überwiegend als Farbstoff für Textilien
und Papier verwendet, aber auch in der Mikroskopie und als Nachweisreagenz für Antimon
eingesetzt. Gesundheitsschädlich.
R 22 -
S 22, 24
weitere Informationen
 01/2006
01/2006
 zurück
zurück
Rizinusöl
Schwach gelbes, viskoses, brennbares, unverdauliches, fettes Öl; wird durch
Kaltpressen der Samen der Rizinusstaude (Ricinus communis) gewonnen.
weitere Informationen
 06/1998 - 03/2002
06/1998 - 03/2002
 zurück
zurück
Saccharose 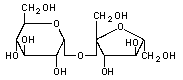 (C12H22O11)
(C12H22O11)
Rohr-, Rüben-, Kristallzucker. Disaccharid aus je einem Molekül
Glucose und Fructose. Bildet farblose Kristalle.
weitere Informationen
 01/1999 - 09/2003 -
03/2004 - 03/2005 -
05/2009 - 06/2013
01/1999 - 09/2003 -
03/2004 - 03/2005 -
05/2009 - 06/2013
 zurück
zurück
Salicylsäure 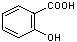 (C7H6O3)
(C7H6O3)
(2-Hydroxybenzoesäure) Weißes geruchloses Pulver. Gut löslich in
Ethanol, Aceton und Diethylether. Die Löslichkeit in Wasser ist stark temperaturabhängig
(bei 20°C 0,2 g / 100 ml, bei 100°C 6 g / 100 ml).
pKS = 2,98. Salicylsäure bildet mit Eisen(III)-Ionen stabile
violette Komplexe. Salicylsäure und einige Derivate wirken analgetisch (schmerzstillend) und
antiphlogistisch (fiebersenkend). Der Essigsäureester gehört zu den wichtigsten
Wirkstoffen: Acetylsalicylsäure (Aspirin®, ASS) Der Methylester der
Salicylsäure, "Wintergrünöl", besitzt einen intensiven Geruch und wird als
Aromastoff verwendet. Salicylsäure ist gesundheitsschädlich, das Pulver
wirkt reizend. R 22
weitere Informationen
 01/2004
01/2004
 zurück
zurück
Salpetersäure, HNO3
Oxidierende anorganische Säure. Stark ätzend.
100%ige Salpetersäure ist farblos, sie zerfällt aber unter Lichteinwirkung
unter Freisetzung von Stickoxiden. Daher ist rauchende Salpetersäure rotbraun
gefärbt und gibt braune Dämpfe ab. Konzentrierte Salpetersäure
ist etwa 65%ig. Konzentrierte Salpetersäure
kann viele organische Verbindungen nitrieren. Darauf beruht die Xanthoproteinreaktion,
die Gelbfärbung von Proteinen beim Kontakt mit konz. Salpetersäure.
R 35 - S 2, 23, 26, 27
weitere Informationen
 05/2000 - 12/2001 -
11/2002 - 09/2003 -
11/2009 - 09/2014
05/2000 - 12/2001 -
11/2002 - 09/2003 -
11/2009 - 09/2014
 zurück
zurück
Salzsäure, HCl
(Chlorwasserstoffsäure), wässrige Lösung von
Chlorwasserstoff (HCl) in Wasser. Es können (bei 25oC) Konzentrationen
bis ca. 38% (= rauchende Salzsäure) erhalten werden. Ätzend.
R 34, 37 - S 2, 26
weitere Informationen
 08/1999 -
02/2000 - 06/2000
- 11/2000 - 12/2001
- 05/2002 - 10/2003
- 12/2003 - 08/2004
- 02/2006 - 11/2007
- 05/2008 - 05/2010
- 07/2011 - 12/2012
- 08/2024
08/1999 -
02/2000 - 06/2000
- 11/2000 - 12/2001
- 05/2002 - 10/2003
- 12/2003 - 08/2004
- 02/2006 - 11/2007
- 05/2008 - 05/2010
- 07/2011 - 12/2012
- 08/2024
 zurück
zurück
Schiffs Reagenz
(Fuchsin-schweflige Säure), Nachweisreagenz auf Aldehyde.
0,17 g Fuchsin in 100 ml Wasser lösen.
30 ml dieser Lösung zu 270 ml schweflige Säure (ca. 5% SO2 in Wasser) geben.
Variante: 0,3 g Fuchsin in 1000 ml lösen und 15 ml einer 38%igen
NaHSO3-Lösung zugeben. 10 Minuten rühren und dann konz.
Salzsäure zutropfen, bis die Lösung farblos ist (ca. 10 ml).
R 20, 34 - S 26, 36/37/39, 45
weitere Informationen
 08/2009
08/2009
 zurück
zurück
Schwefel, S8
Schwefel kommt elementar in Form von leuchtend gelben Kristallen vor.
Im Handel ist er als feines gelbes Pulver, das in Wasser unlöslich,
in den meisten organischen Lösungsmitteln nur wenig löslich ist.
Gut löslich ist Schwefel in Schwefelkohlenstoff (CS2).
An der Luft verbrennt Schwefel unter Bildung von ätzendem SO2.
Auch mit fast allen anderen Elementen werden Verbindungen gebildet, die
Reaktionen laufen dabei teilweise sehr heftig ab.
R 11 - S 16, 23
weitere Informationen
 08/2003
08/2003
 zurück
zurück
Schwefelsäure, H2SO4
Anorganische Säure, konzentriert sehr aggressiv, ätzend.
Zum Verdünnen die Säure vorsichtig, unter Rühren und ggf.
Kühlung, in das Wasser einfließen lassen.
R 35 - S 26, 30, 45
weitere Informationen
 05/1998 - 11/1998 -
12/1998 - 01/1999 -
04/1999 - 10/1999 -
09/2001 - 09/2003 -
12/2003 - 10/2005 -
05/2006 - 11/2007 -
03/2009 - 07/2010 -
02/2012 - 04/2015
05/1998 - 11/1998 -
12/1998 - 01/1999 -
04/1999 - 10/1999 -
09/2001 - 09/2003 -
12/2003 - 10/2005 -
05/2006 - 11/2007 -
03/2009 - 07/2010 -
02/2012 - 04/2015
 zurück
zurück
Seignettesalz  Kaliumnatriumtartrat
Kaliumnatriumtartrat
 12/1999 - 07/2002 -
09/2005 - 05/2007 -
11/2009 - 07/2012 -
07/2025
12/1999 - 07/2002 -
09/2005 - 05/2007 -
11/2009 - 07/2012 -
07/2025 zurück
zurück
Stärke
Amylose, weißes Pulver. Polykondensat der Glucose.
Zur Herstellung einer 0,1%igen Stärke-Lösung 0,5 g Stärke in
500 ml siedendes Wasser einrühren und so lange weiter erhitzen, bis eine
klare Lösung entstanden ist. Frische Stärke-Lösung hält sich
nur einige Tage, denn Mikroorganismen, vor allem Pilze, vermehren sich in dieser
"Nährlösung". Sie kann jedoch durch 1-2 Körnchen
Quecksilberchlorid stabilisiert werden.
weitere Informationen
 12/1998 - 08/1999
- 03/2004 - 08/2007
- 11/2007 - 04/2008
- 08/2008 - 02/2011
- 06/2013
12/1998 - 08/1999
- 03/2004 - 08/2007
- 11/2007 - 04/2008
- 08/2008 - 02/2011
- 06/2013
 zurück
zurück
Strontiumchlorid, SrCl2
Bildet farblose hygroskopische Kristalle; in Wasser sehr gut löslich.
Gesundheitsschädlich.
R 22 -
S 25
weitere Informationen
 12/2014
12/2014
 zurück
zurück
Strontiumnitrat, Sr(NO3)2
Bildet farblose Kristalle, die in Wasser sehr gut löslich sind; in organischen
Lösungsmitteln unlöslich. In der Pyrotechnik wird für Rotfeuer
meist Strontiumnitrat eingesetzt.
Brandfördernd, gesundheitsschädlich, reizend.
R 8, 22, 38 -
S 16, 37/39
weitere Informationen
 01/2000
01/2000
 zurück
zurück
Sudan III 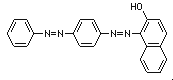 (C22H16N4O)
(C22H16N4O)
"Sudan" ist ein Handelsname der I.G. Farben für fettlösliche,
wasserunlösliche Farbstoffe. Am gebräuchlichsten ist Sudan III (rot).
S 22, 24/25
weitere Informationen
 06/1998 - 02/2002 -
02/2008 - 10/2014 -
02/2017
06/1998 - 02/2002 -
02/2008 - 10/2014 -
02/2017
 zurück
zurück
Sulfanilsäure 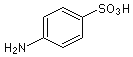 (C6H7NO3S)
(C6H7NO3S)
(4-Amino-benzolsulfonsäure). Bildet farblose Kristalle, die
in Wasser und organischen Lösungsmitteln kaum löslich sind.
Gut löslich nur in Alkalilaugen. Wichtige Ausgangsverbindung für
Azo-Farbstoffe. Reizend.
R 36/38, 43 - S 24, 37
weitere Informationen
 04/1999 - 02/2005 - 12/2013
04/1999 - 02/2005 - 12/2013
 zurück
zurück
Tannine
(Gerbsäure).
Gruppe natürlicher Polyphenole, die sich formal von der
Gallussäure ableiten. Das meist hellgelbe Pulver
besitzt einen schwachen, eigenartigen Geruch und adstringierenden (zusammenziehenden)
Geschmack. Tannin wird hauptsächlich aus Pflanzengallen gewonnen, kommt aber auch
in vielen anderen Pflanzenteilen, besonders in der Rinde von Eichen vor.
Tannine werden zum Gerben von Häuten, zur Herstellung von Eisen-Gallus-Tinte
und in der Heilkunde als Antiseptikum (zur Desinfektion) und Hämostyptikum
(zur Blutstillung) verwendet. Da viele Proteine, Schwermetalle und Alkaloide von
Gerbsäuren ausgefällt werden, kommen Tannine auch zur Klärung von
Getränken sowie bei Vergiftungen zum Einsatz.
weitere Informationen
 06/2000 - 01/2002
- 04/2015
06/2000 - 01/2002
- 04/2015
 zurück
zurück
Tashiro-Mischindikator
Alkoholische Lösung von 0,1% Methylenblau und 0,03%
Methylrot. Indikator für Säure-Base-Titrationen:
pH 4-6 (violett 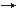 grau
grau  grün)
grün)
 zurück
zurück
Thymolblau  (C27H30O5S)
(C27H30O5S)
(Thymolsulfonphthalein) Braungrünes, in Wasser kaum, in Alkohol und verdünnten Laugen
lösliches Pulver.
Säure-Base-Indikator mit zwei Umschlagbereichen:
pH 1,2-2,8 (rot  gelb),
pH 8,0-9,6 (gelb
gelb),
pH 8,0-9,6 (gelb  blau).
blau).
weitere Informationen
 11/2000 - 02/2009
11/2000 - 02/2009
 zurück
zurück
Thioacetamid 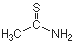 (C2H5NS)
(C2H5NS)
(Thioessigsäureamid) farbloser kristalliner Feststoff; Geruch nach faulen Eiern.
Kommt im Kationen-Trennungsgang zur Fällung von Sulfiden zum Einsatz. Giftig!
R 22, 36/38, 45, 52/53 -
S 45, 53, 61
weitere Informationen
 01/2021
01/2021
 zurück
zurück
Titanoxidsulfat, ZiOSO4 · H2O
(Titanylsulfat) bildet farblose Kristalle, die in Wasser nur wenig, in Säuren gut löslich sind.
Die Chemikalien enthalten in der Regel noch Schwefelsäure, sind daher ätzend.
R 35 -
S 26, 36/37/39, 45
 02/2012
02/2012
 zurück
zurück
Toluol  (C7H8)
(C7H8)
(Methylbenzol) Farbloses, brennbare Flüssigkeit mit benzolartigem Geruch.
Mit Wasser nicht, mit den meisten organischen Lösungsmitteln gut mischbar.
Ausgangssubstanz vieler aromatischer Verbindungen und wichtiges Lösungsmittel.
Leichtentzündlich.
R 11, 20 - S 16, 29, 33
weitere Informationen
 02/2002 - 11/2014
02/2002 - 11/2014
 zurück
zurück
Trichloressigsäure, CHCl2-COOH
(Trichlorethansäure) Farblose Kristalle mit säuerlichem Geruch, Smp. 59°C, gut wasserlöslich.
Ätzend. Wird in 40-80%iger Lösung zum Veröden in der Medizin verwendet (Warzen, Blutungen).
R 10, 25 - S 2, 23, 26
weitere Informationen
 05/2025
05/2025
 zurück
zurück
Triethylamin 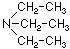 (C6H15N)
(C6H15N)
klare farblose Flüssigkeit, von unangenehmen stark aminartigen Geruch.
Mit kaltem Wasser mischbar, oberhalb von 18,7°C nur wenig in Wasser löslich.
Triethylamin ruft auf der Haut schwere Verätzungen hervor, die Dämpfe
sind stark reizend.
R 11, 36/38 - S 16, 26, 29
weitere Informationen
 07/2004
07/2004
 zurück
zurück
Wasser, H2O
(Dihydrogenmonoxid), anorganisches Lösungsmittel.
weitere Informationen
 zurück
zurück
Wasserstoffperoxid, H2O2
Reines Wasserstoffperoxid ist eine farblose Flüssigkeit, die explosionsartig in
Wasser und Sauerstoff zerfallen kann. Es kommt als wässrige Lösung in unterschiedlicher
Konzentration in den Handel (bis 30% = "Wasserstoffsuperoxid"). Wasserstoffperoxid-Lösungen
werden zur Desinfektion und zum Bleichen verwendet ("Superoxidblond"). Der Zerfall wird von
einigen organischen Stoffen und vielen Schwermetall-Ionen katalysiert. Zur Stabilisierung
werden Wasserstoffperoxid-Lösungen Komplexbildner, z.B. Phosphate, zugegeben.
Wasserstoffperoxid ist Ätzend.
R 34 -
S 3, 28, 36/39, 45
weitere Informationen
 10/1998 - 10/2000
- 07/2001 - 09/2001
- 08/2004 - 01/2006
- 08/2008 - 02/2012
- 12/2012 - 03/2013
- 08/2014 - 04/2016
- 05/2016 - 07/2023
- 08/2023
10/1998 - 10/2000
- 07/2001 - 09/2001
- 08/2004 - 01/2006
- 08/2008 - 02/2012
- 12/2012 - 03/2013
- 08/2014 - 04/2016
- 05/2016 - 07/2023
- 08/2023
 zurück
zurück
Weinsäure 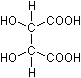 (C4H6O6)
(C4H6O6)
(2,3-Dihydroxybutandisäure, 2,3-Dihydroxybernsteinsäure, Weinsteinsäure),
Organische zweibasige Säure. Die Salze heißen Tartrate. Weinsäure bildet
farblose, gut wasserlösliche Kristalle, die auch in Methanol, Ethanol, Propanol und Glycerin
löslich sind. Die Weinsäure tritt in drei Stereoisomeren auf: L(+)- (= 2R,3R), D(-)
(= 2S,3S) und meso-Weinsäure (2R,3S). L(+)-Weinsäure kommt in vielen Früchten
vor, Kaliumhydrogentartrat scheidet sich als "Weinstein" nach der
Gärung des Weines aus.
weitere Informationen
 01/2002 - 04/2016
01/2002 - 04/2016
 zurück
zurück
Xylole 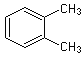 o-Xylol,
o-Xylol,
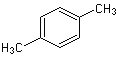 p-Xylol (C8H10)
p-Xylol (C8H10)
(Dimethylbenzol) Alle drei Isomere sind farblose, brennbare, mit wasser nicht, mit den
meisten organischen Lösungsmitteln gut mischbare Flüssigkeiten.
Als Lösungsmittel kommt in der Regel ein Gemisch aller drei Isomere zum Einsatz,
wobei ortho- und para-Xylol üeberwiegen. Leichtentzündlich.
R 10, 20 - S 24/25
weitere Informationen
 02/2002
02/2002
 zurück
zurück
Zink, Zn
Unedles Metall. Wird von Wasser infolge Passivierung kaum angegriffen,
ist jedoch in verdünnten Säuren leicht löslich.
weitere Informationen
 07/1998 - 01/2000 -
05/2003 - 08/2003 -
10/2003 - 04/2005 -
06/2006 - 08/2006 -
02/2012 - 12/2013
07/1998 - 01/2000 -
05/2003 - 08/2003 -
10/2003 - 04/2005 -
06/2006 - 08/2006 -
02/2012 - 12/2013
 zurück
zurück
Zinkchlorid, ZnCl2
Wasserfreies Zinkchlorid ist stark hygroskopisch. Es bildet ein weißes
körmiges Pulver, das an der Luft rasch zerfließt. Sehr gut wasserlöslich,
die Lösungen reagieren sauer; gut löslich in vielen organischen
Lösungsmitteln (Alkohole, Aceton, Diethylether). Aus wässrigen Lösungen
kristallisiert das Tetrahydrat aus. Zink-Ionen sind für Mikroorganismen giftig,
Zinkchlorid wird daher auch als Holzschutzmittel eingesetzt.
R 34 -
S 7/8, 28, 29
weitere Informationen
 12/2004 - 01/2016 -
08/2016
12/2004 - 01/2016 -
08/2016
 zurück
zurück
Zinksulfat, ZnSO4 · 7 H2O
("Zinkvitriol") bildet farblose, gut wasserlösliche Kristalle. Durch Entwässern entsteht
daraus das Monohydrat. Industriell wichtigste Zink-Verbindung; wird auch in der Färberei (als Beizmittel)
und in der Medizin aufgrund seiner bakteriziden und adstrinierenden Wirkng angewendet.
S 22
weitere Informationen
 07/2017
07/2017
 zurück
zurück
Zinn(II)chlorid, SnCl2
bildet weiße Kristalle, die in Wasser, Alkoholen, Ketonen und Ethern löslich
sind. Zinn(II)chlorid kann leicht zu Zinn(IV)-Verbindungen oxidiert werden.
Gesundheitsschädlich.
R 22, 36/37/38, 43 -
S 24/25/26, 37
weitere Informationen
 01/2008
01/2008
 zurück
zurück
Zirkonylchlorid, ZrOCl2·H2O
Zirconium(IV)dichloridoxid Octahydrat) weißes Pulver; in Wasser wenig, in organischen
Lösungsmitteln nicht löslich.
Ätzend.
R 34, 37 -
S 26, 36/37/39, 45
 08/2013
08/2013
 zurück
zurück
Zitronensäure 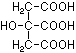 (C6H8O7)
(C6H8O7)
Citronensäure, organische dreibasige Säure. Die Salze heißen Citrate. Zitronensäure bildet
wasserfrei oder als Monohydrat farblose Kristalle die gut wasserlöslich aber nicht
hygroskpisch sind; löslich in Methanol und Ethanol, in den meisten organischen
Lösungsmitteln unlöslich. Sie ist nicht optisch aktiv.
Zitronensäure wird von allen Lebewesen
im Citrat-Zyklus produziert und ist somit an der Energiegewinnung beteiligt. Sie kann
leicht aus Citrusfrüchten isoliert werden. Heute erfolgt die Produktion hauptsächlich
biotechnologisch. Reizend.
R 36 - S 24/25
weitere Informationen
 03/2002 - 03/2004 -
06/2004 - 05/2009 -
10/2009 - 03/2012
03/2002 - 03/2004 -
06/2004 - 05/2009 -
10/2009 - 03/2012
 zurück
zurück
Für den Inhalt externer Seiten wird keine Verantwortung übernommen!
 zurück zum Experiment des Monats
zurück zum Experiment des Monats
Letzte Änderungen am: Freitag, 27. Februar 2026, A. Schunk