

|
Experiment des Monats
|
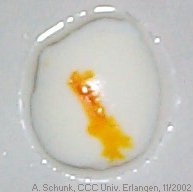
Proteine werden durch konzentrierte Säuren denaturiert (vgl. Experiment 07/2000). Dabei fallen Proteine aus Hühnereiweiß als milchig-weißer Niederschlag aus. Wird konzentrierte Salpetersäure verwendet, beobachtet man eine deutliche Gelbfärbung. Dieser Effekt wird als Xanthoprotein-Reaktion bezeichnet.
 |
 |
Geräte und Chemikalien:
Hühnereier, 0,9%ige Kochsalz-Lösung
konzentrierte Salpetersäure
Reagenzgläser, Petrischale
Durchführung:
Das Eiklar eines rohen Hühnerei (vorsichtig vom Eidotter trennen)
wird in ca. 300 ml isotonischer (0,9%iger) Kochsalzlösung
dispergiert. Ein Reagenzglas zur Hälfte mit dieser kolloidalen
Lösung füllen, ca. 1 ml konz. Salpetersäure
zugeben und schütteln. Es bildet sich ein gelber Niederschlag.
Auf ein gekochtes und geschältes Hühnerei einige Tropfen
konz. Salpetersäure geben. Auch hier erfolgt eine Gelbfärbung.
 |
Erklärung:
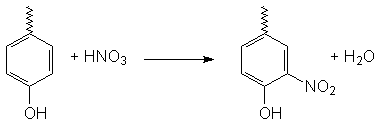
Aromatische Systeme können durch konzentrierte Salpetersäure
nitriert werden. Dies ist auch bei den Phenylresten der Aminosäuren
Phenylalanin und Tyrosin möglich. Die Nitroderivate zeigen
eine intensiv gelbe Färbung.
Gefahren:


Salpetersäure ist ätzend und giftig.
Entsorgung:
Die neutralisierte Lösung kann zum Abwasser gegeben werden,
die mit Säure behandelten Eier kommen zum Hausmüll (nicht essen!).
Literatur & Links:
F. Bukatsch, W. Glöckner: "Experimentelle Schulchemie", Bd. 8, S. 135
K.-H. Grothe: "Chemie", S. 114
Kemper/Fladt: "Chemie", S. 434
Oktober 2002: Der blutende Kastanienzweig
 zurück zum aktuellen Experiment
zurück zum aktuellen Experiment
Seite erstellt am: Donnerstag, 31. Oktober 2002, A. Schunk, CCC Univ. Erlangen.
Für den Inhalt externer Seiten wird keine Verantwortung übernommen!