

|
Experiment des Monats
|
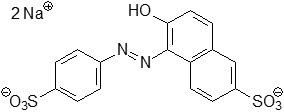
Ostereierfarben sind leicht zugängliche Quellen für verschiedene Lebensmittelfarben - synthetischen oder natürlichen Ursprungs. Kaltfärbetabletten für orange enthalten meistens Gelborange S.
 |
Geräte und Chemikalien:
Ostereierfarbe mit Gelborange S (E 110), Entfärber mit Dithionit (z.B. Dr.Beckmann, Heitmann),
Natriumsulfit, verd. Schwefelsäure,
Bleichmittel auf Chlorbasis (Eau de Javel),
Bechergläser oder Reagenzgläser.
Durchführung:
Die Färbetablette in Wasser auflösen und je eine Probe der Lösung mit Entfärber,
einer Lösung von Natriumsulfit und einigen Tropfen Schwefelsäure bzw. Chlorbleiche versetzen.
Mit dem Bleichmittel erfolgt sofort eine Entfärbung, die Sulfit-haltige Lösung entfärbt
sich langsam, mit dem Entfärber ist keine Farbänderung zu beobachten.
 |
Erklärung:
Gelborange S ist ein Azofarbstoff und lässt sich nicht reduzieren, daher kommt es mit Dithionit zu keiner
Farbänderung. Beim ansäuern von Sulfiten entsteht Schwefeldioxid, das zu einer langsamen Entfärbung
des Farbstoffs führt. Bleichmittel enthalten Hypochlorit oder Peroxide; in beiden Fällen entsteht letztlich
elementarer Sauerstoff, der für die bleichende Wirkung verantwortlich ist.
Gefahren:

Die meisten Bleichmittel und Entfärber wirken reizend, Schwefelsäure ätzend.
Vorsicht: hypochlorithaltige Bleichmittel dürfen nicht angesäuert werden, da sonst Chlorgas entweicht.
Entsorgung:
Die Lösungen werden zum anorganischen Abfall gegeben.
Literatur & Links:
G. Wittke: "Farbstoffchemie"
Lehrbücher zur anorganischen und organischen Chemie
Produktinformationen der Hersteller
 zurück zum aktuellen Experiment
zurück zum aktuellen Experiment
Seite erstellt am: Montag, 25. März 2024,
A. Schunk,
Charité - Universitätsmedizin Berlin.
Für den Inhalt externer Seiten wird keine Verantwortung übernommen!