

|
Experiment des Monats
|
Die Reduktion von Permanganat-Ionen ist abhängig vom pH-Wert. Erkennbar ist dies an den Farbänderungen während der Reaktion. In saurer Lösung entfärbt sich die violette Lösung, im neutralen Medium tritt eine Braunfärbung auf, die basische Lösung wird dunkelgrün.
 |
 |
Geräte und Chemikalien:
Kaliumpermanganat,
Zink,
verdünnte Schwefelsäure,
verdünnte Natronlauge,
Natriumsulfit
Reagenzgläser, Becherglas.
Durchführung:
Drei Reagenzgläser mit 0,1%iger KMnO4-Lösung füllen.
Ein Reagenzglas mit verd. Schwefelsäure (keine Salzsäure verwenden,
da dann Chlorgas entsteht!) ansäuern. In eine Lösung verd. Natronlauge
geben. Zur sauren Lösung etwas Zinkpulver geben. Es beginnt eine lebhafte
Gasentwicklung und die Lösung entfärbt sich. Der neutralen und basischen
Lösung 1%ige Na2SO3-Lösung zugeben. Hier beobachtet
man eine Farbänderung nach braun bzw. grün, wobei sich in der braunen
Lösung ein Niederschlag bildet.
Erklärung:
Die Reduzierbarkeit von Permanganat ist abhängig von der
Protonenkonzentration, und somit vom pH-Wert. In saurer Lösung
erfolgt die Reduktion von der Oxidationsstufe +VII (Permanganat) zu +II
(Mn2+). In neutraler Lösung endet die Reduktion bei
+IV (Mn(OH)4 bzw. MnO2 = Braunstein), in basischer
Lösung entsteht Manganat(VI) (MnO42-):
| sauer: | MnO4- + 5 e- + 8 H+ | 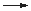 |
Mn2+ + 4 H2O |
| neutral: | MnO4- + 3 e- + 4 H+ | 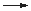 |
MnO2 + 2 H2O |
| basisch: | MnO4- + e- | 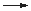 |
MnO42- |
In der sauren Lösung entsteht aus Zink + Schwefelsäure Wasserstoff, der das Permanganat reduziert. Sulfit (SO32-) wird zu Sulfat (SO42-) oxidiert. Alternativ können auch andere Reduktionsmittel verwendet werden, z.B. Ascorbinsäure, FeSO4, Glucose (in basischer Lösung). Wird Zink in die basische Lösung gegeben, erfolgt eine direkte Reduktion des Permanganats durch Zink, es entsteht kein Wasserstoff.
Gefahren:


Schwefelsäure und Natronlauge sind ätzend,
Kaliumpermanganat ist brandfördernd und gesundheitsschädlich
Entsorgung:
Die Lösungen kommen zum Schwermetall-Abfall.
Literatur & Links:
Lehrbücher der Anorganischen Chemie
 zurück zum aktuellen Experiment
zurück zum aktuellen Experiment
Seite erstellt am: Donnerstag, 31. März 2005, A. Schunk, GDCh, Frankfurt/Main.
Für den Inhalt externer Seiten wird keine Verantwortung übernommen!