

|
Experiment des Monats
|
Es muß nicht immer Rotkohl sein ... Auch viele andere Pflanzenfarbstoffe sind in saurer und basischer Lösung unterschiedlich gefärbt, können also als Säure-Base-Indikator verwendet werden. Das Farbenspiel des Extraktes aus Pfingstrosen-Blüten wurde auch von GOETHE beschrieben.
 |
 Bildquelle: Alexandras schöner kleiner Garten |
Geräte und Chemikalien:
getrocknete Blütenblätter roter Pfingstrosen
verdünnte Salzsäure,
verdünnte Natronlauge;
großes Becherglas, Erlenmeyerkolben.
Durchführung:
Blütenblätter roter Pfingstrosen trocknen.
Die getrockneten Blätter in einem Becherglas oder Metalltopf
mit Wasser bedecken und ca. 10 Minuten auskochen.
Den abgekühlten bräunlichen Absud filtrieren und auf drei Kolben
verteilen. Zu einer Lösung etwas Salzsäure geben, es
erscheint ein leuchtendes Rot. Bei Zugabe von Natronlauge
färbt sich die Lösung olivgrün-blaugrün.
Erklärung:
Die färbenden Substanzen in den Pfingstrose-Blüten
gehören zur Gruppe der Anthocyane.
Dies sind Glykoside bestimmter Flavone.
Diese können, abhängig vom pH-Wert, in einer kationischen, neutralen
oder anionischen Form vorliegen, die jeweils unterschiedlich
gefärbt sind:
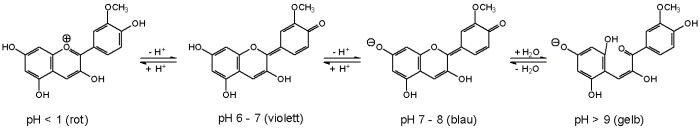
Der Hauptfarbstoff in der Pfingstrose ist das Paeonidin.
Auch die Blütenblätter von Malven und Hibiskus
(Malven- bzw. Hibiskustee), Kornblumen und roten Rosen und einige
Früchte (Kirschen, Pflaumen, Brombeeren, Himbeeren u.a.)
enthalten Anthocyane, die im sauren Bereich rot, im basischen
blau - grün gefärbt sind.
Gefahren:

Salzsäure und Natronlauge sind ätzend.
Entsorgung:
Die Lösungen können dem Abwasser beigegeben werden.
Literatur & Links:
Georg Schwedt: "Goethes chemische Experimente"
- Versuch 21, S. 65
F. Bukatsch, O. Krätz, G. Probeck, R. Schwankner:
"So interessant ist Chemie" - S. 38-42
April 2002: Das Portwein-Wunder
 zurück zum aktuellen Experiment
zurück zum aktuellen Experiment
Seite erstellt am: Dienstag, 30. April 2002, A. Schunk, CCC Univ. Erlangen.
Für den Inhalt externer Seiten wird keine Verantwortung übernommen!