
Experiment des Monats
April 2000
Enol-Titration nach K. H. Meyer

|
Experiment des Monats |
Aldehyde und Ketone stehen in wässriger Lösung im Gleichgewicht mit ihrer Enol-Form ("Keto-Enol-Tautomerie"). Bei Aceton liegt das Gleichgewicht fast vollständig auf der Seite des Ketons. Bei Acetessigester beträgt der Anteil des Enols etwa 7,5%. Die hier gezeigte Reaktion wurde 1912 von KURT H. MEYER zur Bestimmung des Enolgehalts verwendet.



Geräte und Chemikalien:
Reagenzglas, Becherglas mit Eiswasser, Becherglas mit warmem Wasser (ca. 60oC).
Acetessigester,
salzsaure 0,05-molare Eisen(III)chlorid-Lösung,
Bromwasser (oder
Jodlösung).
Durchführung:
5 ml einer 1%igen Lösung von Acetessigester in Wasser in ein Reagenzglas
geben und 5 Tropfen FeCl3-Lösung zufügen. Die Lösung
färbt sich dunkelrot. (I) Die Lösung in Eiswasser abkühlen
(< 3oC) und Bromwasser bis zur Entfärbung zutropfen. (II)
Wird die Flüssigkeit erwärmt, tritt erneut eine Rotfärbung ein. (III)
Nach Abkühlung kann wieder durch eine Bromwasserzugabe entfärbt werden usw..
Erklärung:
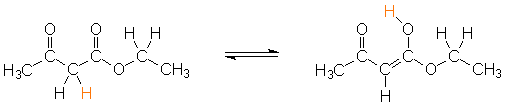
Acetessigester steht in wässriger Lösung im Gleichgewicht mit
seinem Enol, wobei etwa 7,5% der Ester-Moleküle in der Enol-Form
vorliegen.
Gefahren:


Brom (Bromwasser) und Salzsäure sind ätzend. Eingeatmete Bromdämpfe
führen zu schweren Lungenschäden  mit Bromwasser nur im Abzug arbeiten.
mit Bromwasser nur im Abzug arbeiten.
Entsorgung:
Die Lösungen kommen zum organischen Lösungsmittelabfall.
Literatur & Links:
"Chemisches Praktikum für Mediziner" -
CCC, Institut für Organische Chemie der Univ. Erlangen-Nürnberg
Versuch 8.2
H. Beyer, H. Walter, W. Francke: "Lehrbuch der Organischen Chemie" -
Stuttgart, Leipzig: Hirzel, 1998 (23. Aufl.) - S. 312-313
Organikum, 18. Aufl. (1990), S. 476
Herrn Professor i.R. Dr. Hans Hofmann, Bamberg / Erlangen und Frau Dipl.-Chem. Gisela Martinek, Univ. Erlangen-Nürnberg danke ich sehr herzlich für die Hinweise.
März 2000: Herons Sonnenbrunnen
 zurück zum aktuellen Experiment
zurück zum aktuellen Experiment
Seite erstellt am: Freitag, 31. März 2000, A. Schunk.