

|
Experiment des Monats
|
Riboflavin ist ein wasserlösliches Vitamin, es gehört zum
"Vitamin B2-Komplex", zu dem auch Folsäure, Nicotinsäureamid
und Pantothensäure gerechnet werden. Riboflavin ist in fast
allen Nahrungsmitteln enthalten. Besonders reich an diesem Vitamin sind Milch
(daher der alte Name "Lactoflavin"), Pilze, Nüsse und Leber.
Getreidekörner sind vitaminarm, erst bei der Keimung wird Riboflavin gebildet.
Riboflavin wird zur Bildung der Coenzyme FMN (Flavin-Mononucleotid)
und FAD (Flavin-Adenin-Dinucleotid) benötigt, die als prosthetische
Gruppen an wasserstoffübertragenden Enzymen ("Flavo-Proteine") gebunden sind.
Ein Riboflavin-Mangel ist in Europa sehr selten. In einigen tropischen
Gebieten tritt jedoch die
Ariboflavinose
auf.
Das orange-gelbe Riboflavin ist auch als Lebensmittelfarbstoff zugelassen. (E 101)
Es ist unter anderem der Hauptfarbstoff in Vanille-Puddingpulver. Aus diesem kann das
Vitamin leicht extrahiert werden.
 |
 |
 |
Geräte und Chemikalien:
Becherglas, Erlenmeyer- oder Rundkolben, UV-Lampe
Puddingpulver Vanille-Geschmack,
gesättigte Natriumdithionit-Lösung
(ca. 2 g in 10 ml, frisch bereitet).
Durchführung:
8 g Vanille-Puddingpulver in 200 ml Wasser aufschlämmen, (1)
einige Minuten rühren und in einen weithalsigen Kolben abfiltrieren. (2)
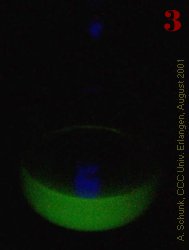
Wird diese Lösung (im Dunkeln) mit einer UV-Lampe bestrahlt, zeigt sie eine
gelb-grüne Fluoreszenz. (3) Nun wird tropfenweise eine gesättigte
Natriumdithionit-Lösung zugegeben, bis die Fluoreszenz erlischt.
Beim Schwenken des unverschlossenen Kolbens kehrt die Fluoreszenz zurück.
Erklärung:
Riboflavin zeigt beim Bestrahlen mit ultraviolettem Licht eine gelb-grüne
Fluoreszenz. Wird das Vitamin reduziert, beispielsweise mit Natriumdithionit,
erlischt die Fluoreszenz. Die Reaktion ist reversibel, durch Luftsauerstoff
kann die Verbindung wieder oxidiert werden.
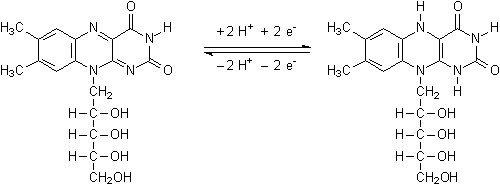
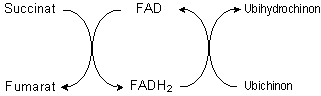
Auf dieser Redox-Reaktion beruht die biochemische Funktion des Riboflavins. Die Coenzyme FMN und FAD, die jeweils eine Riboflavin-Baugruppe enthalten, dienen in der Zelle als Redox-Systeme, beispielsweise beim Zitronensäurezyklus und in der Atmungskette. Im Zitronensäurezyklus wird bei der Oxidation von Succinat zu Fumarat FAD zu FADH2 reduziert. In der Atmungskette wird dieses FADH2 wieder oxidiert und dabei Ubichinon reduziert.
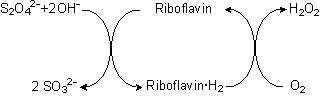
Das Experiment kann als ein Modellversuch für die Funktionsweise von FAD dienen. Riboflavin wird durch Dithionit reduziert, hierbei entsteht Sulfit. Anschließend wird das Vitamin durch Luftsauerstoff wieder oxidiert. Es überträgt also Reduktionsäquivalente von Dithionit auf Sauerstoff.
Gefahren:

Natriumdithionit ist reizend.
Entsorgung:
Die Lösungen kommen zum Abwasser.
Literatur & Links:
Laier, Bettina; Pfeifer, Peter: "Riboflavin";
Naturwissenschaften im Unterricht - Chemie, 7 (1996), Nr. 31, 28/29
Dr. Sabine Bieg, Univ. Mainz, persönliche Mitteilung
 zurück zum aktuellen Experiment
zurück zum aktuellen Experiment
Seite erstellt am: Dienstag, 31. Juli 2001, A. Schunk, CCC Univ. Erlangen.
Für den Inhalt externer Seiten wird keine Verantwortung übernommen!