

|
Experiment des Monats
|
Proteine verändern ihre Struktur, wenn sich das pH-Milieu stark verändert - sie denaturieren. Gelöste Proteinen fallen dann zumeist aus. Auch bei unlöslichen Proteinen lassen sich die Strukturänderungen oft sichtbar machen.
 |
Geräte und Chemikalien:
Batik-Seide (feines Seidengewebe),
konz. Salpetersäure,
Tropfpipette, Glasschale.
Durchführung:
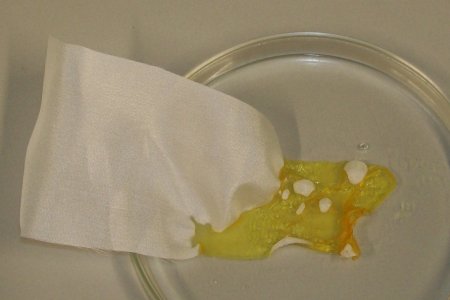
Auf ein Stück Batik-Seide werden einige Tropfen konz. Salpetersäure gegeben.
Es tritt sofort eine Gelbfärbung ein und das Gewebe zieht sich zusammen.
Erklärung:
Seide besteht aus Proteinfasern, die von "Seidenraupen" (den Larven des Seidenspinners)
erzeugt werden. Hauptbestandteil (70-80%) ist das mit den Keratinen verwandte Fibroin, das aus langen
Ketten einfacher Aminosäuren (im wesentlichen Alanin, Glycin und Serin) besteht. Die Fibroin-Fasern
werden durch Sericin verklebt. Dieses Protein enthält auch aromatische Aminosäuren
(insbes. Tyrosin). Daher ist die Xanthoprotein-Reaktion ( EdM 11/2002) positiv = Gelbfärbung. Die starke Säure führt
ausserdem zu einer Konformationsänderung der Proteine, wobei diese Denaturierung zu einer deutlichen
Verformung des Gewebes führt.
EdM 11/2002) positiv = Gelbfärbung. Die starke Säure führt
ausserdem zu einer Konformationsänderung der Proteine, wobei diese Denaturierung zu einer deutlichen
Verformung des Gewebes führt.
Gefahren:

Salpetersäure ist ätzend und giftig.
Entsorgung:
Das ausgespülte Gewebe kann zum Hausmüll gegeben werden.
Säure-Reste werden neutralisiert zum Schwermetall-Abfall gegeben.
Literatur & Links:
RÖMPP Chemie-Lexikon
eigene Unterlagen
August 2014: pH-Abhängigkeit der Katalase-Aktivität
 zurück zum aktuellen Experiment
zurück zum aktuellen Experiment
Seite erstellt am: Samstag, 20. September 2014,
A. Schunk,
Charité - Universitätsmedizin Berlin.
Für den Inhalt externer Seiten wird keine Verantwortung übernommen!